
����Ŀ��2020���¹ڷ���������ȫ���㱬��������״�����������ߺ������У�56������30���ӡ��ƾ�����������������������Ⱦ�����Ч�����������й�˵����ȷ����( )
A.84����Һ����Ч�ɷ���![]()
B.84����Һ��ƾ����ʹ�ÿ���ǿ����Ч��
C.������ɱ����������Ϊ���������ȷ�������
D.�۱�ϩ��֬�������IJ����ֵij�ʼԭ��֮һ���۱�ϩ����ʹ���Ը��������Һ��ɫ
���𰸡�C
��������
A��84����Һ����Ҫ��Ч�ɷ���NaClO����A����
B��84����Һ����ǿ�����ԣ��ƾ����л�ԭ�ԣ�����ϻ���Ϊ����������ԭ��Ӧ����������Ч������B����
C����ʹ�����ʱ��Եķ����и��¼��ȡ����������䡢�������ȣ������ijɷ��ǵ����ʣ�������ʹ�����ʱ��ԣ�������ɱ������C��ȷ��
D���۱�ϩ�ṹ�в�����̼̼˫��������ʹ���Ը��������Һ��ɫ����D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǵؿ��к�������Ԫ�أ����ǿ����к�������Ԫ�ء�
��1��H2O�е�O-H�������Ӽ�ķ��»����������ǿ������˳������Ϊ____>___>___��
��2��![]() �ķе����
�ķе���� ����ԭ����____��
����ԭ����____��
��3��O��S��Se�����ڵڢ�IA��Ԫ�أ��γɼ��⻯��ķе��ɸߵ��͵�˳��Ϊ____>____>____�������ʽ����
��4����ͼ1��ʾij�ֺ����л�������Ľṹ��ʽ���������4����ԭ�ӷֱ�λ�����������4�����㣨��ͼ2���������ڴ��ڿ�ǻ����Ƕ��ij�����ӻ���Ӳ��γ�4���������ʶ��
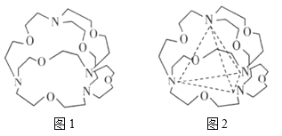
���з��ӻ������У��ܱ����л�������ʶ�����____�����ţ���
A.CF4 B.NH4+ C.CH4 D.H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤Cl2��Fe3+��I2���������Ե����ǿ����ijС������ͼ��ʾװ�ý���ʵ��(�г���������ȥ���������Ѽ���)��
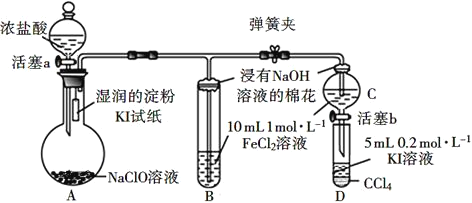
ʵ����̣�
��.���ɼУ�����a���μ�Ũ���ᡣ
��.��B��C�е���Һ����Ϊ��ɫʱ���н����ɼС�
��.��B�м���һ����KSCN��Һ�����Һ�Ժ�ɫ��һ��ʱ���B����Һ��ɫ����رջ���a��
��.����
��1��A�в�������ɫ���壬д��A�з�����Ӧ�Ļ�ѧ��Ӧ����ʽ��___��
��2����֤������������ǿ�ڵⵥ�ʵ�ʵ��������___��
��3��B����Һ������Ӧ�����ӷ���ʽ��___��
��4��Ϊ��֤Fe3+��������ǿ�ڵⵥ�ʣ����̢��IJ�����������___����Ӧ��Ӧ�����ӷ���ʽ��___��
��5����������������Һ����������__��
��6�����̢�ʵ���Ŀ����__��
��7����������ͨ����ɫ�⻯����Һ�У���ɫ��Һ�ȱ�Ϊ��ɫ������ͨ����������Һ�ֱ�Ϊ��ɫ����֪ÿ1molKI��ȫ��Ӧת��6mol���ӣ�д������������⻯����Һ��Ӧ�����ӷ���ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������֬��Ϳ�ϡ���ī�����ᡢ��ճ����Ƥ����������������л��ܼ��������������������Ϊԭ���Ʊ�ȼ���Ҵ�����֪�����������������ͼ״�����������Ӧ�õ�����ش��������⣺
(1)��CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) H1=-874.5kJ/mol
��2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) H2=-1453kJ/mol
��2CH3COOCH3(l)+7O2(g)=6CO2(g)+6H2O(l) H3=-3189.8kJ/mol
��������Ӧ�������CH3COOH(l)+CH3OH(l)=CH3COOCH3(l)+H2O(l)��H=________![]() ��
��
(2)���ڷ�ӦCH3COOH(l)+CH3OH(l)CH3COOCH3(l)+H2O(l)���ж�����ѡ������������ƽ��ת���ʵ���______
A.������������췴Ӧ����
B.��������ļ״�
C.�������������
D.�������������ϵ�з���
E.�ʵ�����߷�Ӧ�¶�
F.�ʵ��ؽ��ͷ�Ӧ�¶�
(3)�ڸ�������ѹǿΪ1.01MPaʱ����������������Ʊ��Ҵ�������������Ӧ��
����Ӧ��CH3COOCH3(g)+2H2(g) CH3OH(g)+CH3CH2OH(g) H<0��
����Ӧ��CH3COOCH3(g)+H2(g) CH3OH(g)+CH3CHO(g) H>0��ʵ���ã�����ͬʱ���ڣ���Ӧ�¶���CH3CH2OH��CH3CHO�IJ���֮��Ĺ�ϵ��ͼ��ʾ��
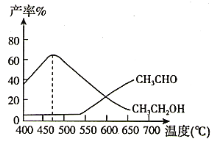
����540��֮ǰCH3CHO�IJ���Զ����CH3CH2OH���ʵ�ԭ����________��
����470��֮��CH3CHO��CH3CH2OH���ʱ仯���ƿ��ܵ�ԭ����________��
(4)����470��ʱ����n(CH3COOCH3):n(H2)=1:10��Ͷ�ϱ�ֻ��������Ӧ(�����Ǹ���Ӧ)���������ת������������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
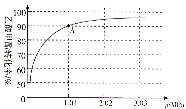
��A��ʱ��CH3COOCH3(g)��ƽ���ѹΪ________MPa��CH3CH2OH(g)���������________%(����һλС��)��
��470��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Kp=________(MPa)-1(KpΪ�Է�ѹ��ʾ��ƽ�ⳣ�����г�����ʽ����Ҫ�������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(Mn3O4)�㷺Ӧ�����������Ų��ϡ��������Ʊ�����һ���Ե�Ʒλ�̿�(��MnCO3��Mn2O3��MnOOH������Fe2O3��Al2O3��SiO2)Ϊԭ������Mn3O4�Ĺ���������ͼ��
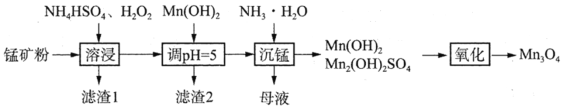
��֪��![]()
�ش��������⣺
(1) MnOOH��MnԪ�صĻ��ϼ�Ϊ________��
(2)���ܽ�����H2O2��������________��
(3)������2������Ҫ�ɷ���________��
(4)��ĸҺ�������ʵ���Ҫ�ɷ���________��ѭ�����ø����ʵķ�����________��
(5)��������ʱ�����������ˮ�У�70��ˮԡ���ȣ�ͨ����������������ȫ��ת��ΪMn3O4��Mn(OH)2����Mn3O4��Ӧ�Ļ�ѧ����ʽΪ________����Ӧ����Һ��![]() ________(����������������С������������)��
________(����������������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������ܴﵽ��Ӧʵ��Ŀ�ĵ���( )
ѡ�� | ʵ��Ŀ�� | ʵ����� |
A | ���� | �Ƚ� |
B | �Ƚϴ�����̼�����Ե�ǿ�� | �� |
C | ������Һ���Ƿ��� | ȡ�����Լ����Թ��У�����Ũ |
D | ����ϴ������ʵ�������Թ� | ���þƾ���ϴ������ˮ��ϴ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����缫���ˮ�����װ����ͼ�����缫Ϊ���缫a�����缫b��Ni(OH)2�缫��ͨ�����ƿ�������K1��K2���ɽ���õ�H2��O2������˵��������ǣ� ��
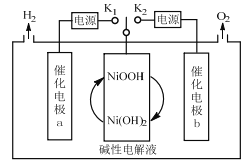
A.��O2ʱ��������Ni(OH)2�缫ͨ�����·������缫b
B.��H2ʱ�������ĵ缫��ӦʽΪNi(OH)2+OH--e-=NiOOH+H2O
C.���缫b�ϣ�OH-����������Ӧ����O2
D.��װ�ÿ�����Ĥ���������Ʊ��ߴ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֽ�������AgCl�ֱ�������������У�AgCl���ܽ���ɴ�С��˳����
��20mL 0.01mol��L��1 KCl��Һ ��30mL 0.02mol��L��1 CaCl2��Һ��40mL 0.03mol��L��1 HCl��Һ
A.��>��>��B.��>��>��C.��>��>��D.��>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����Ԫ����H2Y��Һ�еμ� KOH ��Һ�����û����Һ�� pH �� P[P��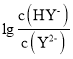 ��
��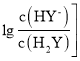 �仯��ϵ��ͼ��ʾ������˵����ȷ����
�仯��ϵ��ͼ��ʾ������˵����ȷ����
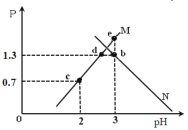
A.���� M ��ʾ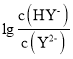 �� pH �ı仯��ϵ
�� pH �ı仯��ϵ
B.Ka2 ����ֵ��10-6
C.e ����Һ�У�2c(Y2-)+c(HY-)��c(K+)+c(OH-)=0.001mol��L-1
D.KHY ��Һ�У�c(K��)��c(HY��)��c(H+)��c(Y2-)��c(H2Y)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com