
【题目】我国古代劳动人民在生产生活中积累了丰富的经验,很多生产过程的操作方法与化学实验中的物质分离除杂方法相似。下列加有着重号的文字与对应分离方法正确的是( )
《本草集经注》 | 《通州煮海录》 | 《名医别录》 | 《续遵义府志》 |
凡渍药酒,皆须细切……便可漉出 | 海陆取卤,日晒火煎,煮海熬波,卤水成盐 | 凡煮汤,欲微火,令小沸……箅渣取液 | 经月画出蒸之……终乃得酒可饮 |
|
|
|
|
A.过滤、蒸馏、萃取、蒸发B.过滤、蒸发、萃取、蒸馏
C.蒸发、萃取、蒸馏、过滤D.萃取、蒸发、过滤、蒸馏
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某探究小组用碘量法来测定样品中N2H4·H2O的含量。取样品5.000 g,加水配成250 mL无色溶液,已知溶液呈碱性,取25.00 mL溶液,用滴定管盛装0.2000 mol/L的I2标准液进行滴定。滴定反应中氧化产物和还原产物分别为N2和I-。
(1)用_____________填“酸式”或“碱式”)滴定管盛装I2标准液,在取液、盛装、滴定过程中还需要的玻璃仪器有_____________________________________。
(2)滴定过程中,需要加入_____作为指示剂,滴定终点的判断方法___________。
(3)滴定前后液面如图所示,所用I2标准液的体积为________________mL。

(4)样品中水合肼(N2H4·H2O)的质量分数为_____________________,若滴定过程中,盛放I2标准液的滴定管刚开始有气泡,滴定后无气泡,则测得样品中水合肼(N2H4·H2O)的质量分数____________填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用乙醇与浓硫酸的混合液加热的方法制取乙烯。反应中常因温度而发生副反应。请选用下列装置(装置可以使用多次)完成相关实验并回答有关问题:

(1)制备乙烯时,常在A装置的烧瓶中加入碎瓷片,其目的是__________;加热时要使溶液的温度迅速上升到140℃以上,因为在140℃左右易生成乙醚,该有机物的结构简式为__________;生成乙烯的化学方程式为___________。
(2)乙醇与浓硫酸加热制取乙烯时,乙烯气体中常混有SO2和CO2,为验证有副产物SO2和CO2气体存在,上述仪器的连接顺序为a→__________。
(3)某同学设计制备1,2-二溴乙烷的装置连接顺序为A→E→C→D。已知1,2-二溴乙烷的主要物理性质有:难溶于水、熔点9℃、沸点132℃、密度2.2g·cm-3。
①E装置的作用__________。
②分离D装置中1,2-二溴乙烷的操作方法是加入试剂__________,充分反应后进行__________操作。
③反应过程中,应将D装置放在10℃的水浴中,温度不宜过低、过高的原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是

A. 反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 图中X点所示条件下,延长反应时间能提高NO转化率
C. 图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
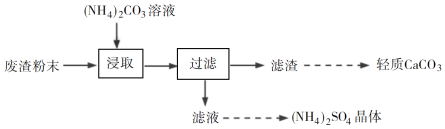
(1)室温下,反应CaSO4(s)+![]() (aq)
(aq)![]() CaCO3(s)+
CaCO3(s)+![]() (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中 =________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
=________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为________;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是________。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________。

(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:______[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E五种短周期元素,其中A,B,C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D,E原子核内各自的质子数与中子数相等;B元素可分别与A,C,D,E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为 7∶8,E与B的质量比为1∶1。试回答:
(1)写出D元素基态原子的电子排布式:__________________________。
(2)写出AB2的结构式:___________________________________________________。
(3)B,C两元素的第一电离能大小关系为______>______(填元素符号),原因是____________________。
(4)根据VSEPR模型预测C的氢化物的立体构型为____________,中心原子C的杂化轨道类型为________。
(5)C的单质分子中π键的数目为______,B,D两元素的气态氢化物的稳定性大小关系为______>____(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池可用于有机废水的处理,如图是利用微生物处理含尿素[CO(NH2)2]废水的装置。下列说法中正确的是

A. 该装置外电路中箭头的方向代表电流的方向
B. M电极反应式为CO(NH2)2-6e-+H2O=CO2↑+6H++N2↑
C. 当有1mlH+通过质子交换膜时,N极消耗5.6LO2
D. 该处理工艺会导致废水酸性增强,仍旧不能直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量Cl2,溶液中某些离子的物质的量变化如下图所示。下列说法中,不正确的是

A. 还原性:I->Fe2+>Br-
B. 原混合溶液中FeBr2的物质的量为3mol
C. 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
D. 当通入3mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s) + 2NO(g) ![]() CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是
CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是

A. 该反应的△H>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 若状态B、C、D的压强分别为PB、PC 、PD ,则PC=PD>PB
D. 在T2时,若反应体系处于状态D ,则此时v正>v逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com