
【题目】向含溶质0.2mol的Al2(SO4)3溶液中加入1000mL KOH溶液,生成白色沉淀7.8g ,则KOH溶液的物质的量浓度可能为
A.0.3mol/L B.0.7mol/L C.0.8 mol/L D.1.5mol/L
【答案】AD
【解析】
试题分析:1、若氢氧化钠不足量,氢氧根全部转化为沉淀。
设 KOH溶液的物质的量浓度是amol/L,则
3OH-+Al3+=Al(OH)3↓
3 78g
amol 7.8g 得a=0.3
2、若硫酸铝不足量,先生成沉淀,后沉淀部分溶解。
硫酸铝中Al3+的物质的量为2×0.2mol=0.4mol,7.8g沉淀需要Al3+的物质的量为0.1mol,则转变成AlO2-的Al3+的物质的量为0.3mol。设KOH溶液的物质的量浓度是bmol/L,则
3OH- + Al3+=Al(OH0.3mol 0.1mol)3↓
3 mol 1mol
4OH- + Al3+=AlO2-+2H2O
4mol 1mol
1.2mol 0.3mol
所以KOH溶液的物质的量浓度是b=![]() =1.5mol/L
=1.5mol/L


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中固体剩余物是( )
A. Na2CO3和Na2O2 B. Na2CO3和NaOH
C. NaOH和Na2O2 D. NaOH、Na2O2和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知同温同压下,气体的密度与它的摩尔质量成正比。一只气球若放在空气(空气的平均摩尔质量约为29g/mol)中可静止不动,则相同条件下该气球放在下列气体中会下沉的是
A. NO2 B. Cl2 C. CO2 D. CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在容积不变的密闭容器中注满NO2气体,2NO2(g)N2O4(g)△H<0.平衡后把该容器置于冰水中,下列性质或数值不会改变的是( )
①平均摩尔质量 ②质量 ③颜色 ④压强 ⑤各组分的质量分数⑥密度.
A.②⑥
B.②③
C.④⑤
D.①⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( ) 
A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时未达到化学平衡
C.升高温度,平衡会向正反应方向移动
D.该反应的正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟工业制漂白粉,设计了如下图所示的实验装置。己知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O

回答下列问题:
(1)甲装置中仪器a的名称是_________________,MnO2在反应中所起的作用是_____________。
(2)装置乙中饱和食盐水的作用是_________________。
(3)①制取漂白粉的化学方程式是____________________。
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是____________________。
③为提高Ca(ClO)2的含量,可采取的措施是___________________(任写一种即可)。
(4)漂白粉应密封保存,原因是__________、_________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组的同学设计了如下实验装置制备SnCl4。
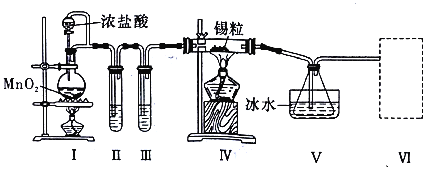
已知:①金属锡熔点为231℃,化学活泼性与铁相似;
②纯净而干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4的沸点为114℃;
③SnCl4易与水反应。
请根据上图装置回答:
(1)裝置I中发生反应的离子方程式是______________。
(2)试管II中的试剂是________,试管III中的试剂是____________。
(3)装置V的作用是____________。
(4)裝置Ⅵ 最好选用下列装置中的____(填标号)。
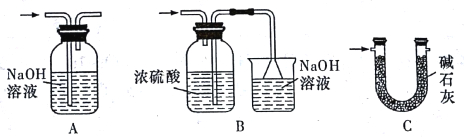
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com