
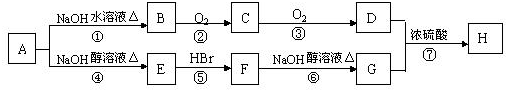
���� �л���A�������ΪC4H9Br����������һ����֧����A�ܺ�NaOH��ˮ��Һ����ȡ����Ӧ����B��BΪ����B�ܷ�������������Ӧ����D��DΪ���ᣬ��B�д���-CH2OH�ṹ������AΪ��CH3��2CHCH2Br��BΪ��CH3��2CHCH2OH��CΪ��CH3��2CHCHO��DΪ��CH3��2CHCOOH��A������ȥ��Ӧ����EΪ��CH3��2C=CH2��E���廯�ⷢ���ӳɷ�Ӧ����F�������Ϣ�ٿ�֪��F�Ľṹ��ʽΪ��CH3��3CBr��F����ˮ�ⷴӦ����GΪ��CH3��3COH��D��F����������Ӧ����HΪ��CH3��2CHCOOC��CH3��3���ݴ˽��
��� �⣺�л���A�������ΪC4H9Br����������һ����֧����A�ܺ�NaOH��ˮ��Һ����ȡ����Ӧ����B��BΪ����B�ܷ�������������Ӧ����D��DΪ���ᣬ��B�д���-CH2OH�ṹ������AΪ��CH3��2CHCH2Br��BΪ��CH3��2CHCH2OH��CΪ��CH3��2CHCHO��DΪ��CH3��2CHCOOH��A������ȥ��Ӧ����EΪ��CH3��2C=CH2��E���廯�ⷢ���ӳɷ�Ӧ����F�������Ϣ�ٿ�֪��F�Ľṹ��ʽΪ��CH3��3CBr��F����ˮ�ⷴӦ����GΪ��CH3��3COH��D��F����������Ӧ����HΪ��CH3��2CHCOOC��CH3��3��
��1��������������֪��A�Ľṹ��ʽΪ��CH3��2CHCH2Br��B-H�У��л���FΪ��CH3��3CBr����A��Ϊͬ���칹�壬
�ʴ�Ϊ����CH3��2CHCH2Br��F��
��2������ת���Тڢ�����������Ӧ����������ȥ��Ӧ�������ڼӳɷ�Ӧ���٢ޢ�����ȡ����Ӧ��
�ʴ�Ϊ���٢ޢߣ�
��3��������������֪��C�Ľṹ��ʽΪ����CH3��2CHCHO��
�ʴ�Ϊ����CH3��2CHCHO��
��4����Ӧ�ܵĻ�ѧ����ʽΪ����CH3��2CHCH2Br+NaOH$��_{��}^{��}$��CH3��2C=CH2+NaBr+H2O��
�ʴ�Ϊ����CH3��2CHCH2Br+NaOH$��_{��}^{��}$��CH3��2C=CH2+NaBr+H2O��
���� ���⿼�����л�����ƶϣ��ؼ��ۺϷ���ȷ��A�Ľṹ��ʽ���ٽ��ת����ϵ�ƶϣ���Ҫѧ���������չ����ŵ�������ת�����Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�¶�/�� ������ | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| ������ | Zn��OH��2 | Fe��OH��2 | Fe��OH��3 |
| Ksp����ֵ | 10-17 | 10-17 | 10-38 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
��� ѡ�� | ������ | ����� | ����� | �ǵ���� |
| A | ������ˮ | ���� | Һ̬KNO3 | ���� |
| B | CaO | �� ˮ | ͭ | �Ҵ� |
| C | ���� | ���Ͻ� | AgCl | CO2 |
| D | �������� | ���� | Na2SO4��Һ | ʳ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 14�� | C�� | 10�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��10��104��109 | B�� | 1��5��5��109��5��108 | C�� | 1��20��1010��109 | D�� | 1��10��1010��109 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܢݢޢ� | B�� | �ܢݢ� | C�� | �ڢܢ� | D�� | �ڢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
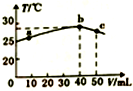
| A�� | 25��ʱ��HA�ĵ���ƽ�ⳣ��KaԼΪ1.43��10-3 | |
| B�� | a��b�Ĺ����У���Һ��c��A-����c��HA��֮��ʼ�ղ��� | |
| C�� | b��c�Ĺ����У��¶Ƚ��͵���Ҫԭ������Һ�з��������ȷ�Ӧ | |
| D�� | ��Ũ�ȵ�NaOH��NaA�����Һ��һ�����ڹ�ϵ��c��Na+����c��A-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com