
| A、AgNO3 |
| B、FeSO4 |
| C、MgCl2 |
| D、(NH4)2SO3 |


科目:高中化学 来源: 题型:
| A、NaI固体 |
| B、K2SO4固体 |
| C、NaOH固体 |
| D、HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4溶液能产生丁达尔效应 |
| B、分散质粒子的直径:浊液>胶体>溶液 |
| C、可以用过滤的方法除去氢氧化铁胶体中的可溶性杂质 |
| D、在饱和氯化铁溶液中滴加氢氧化钠溶液可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
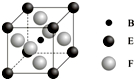 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+ |
| B、Al3+ |
| C、AlO2- |
| D、Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液中可能大量存在Al3+、NH4+、Cl?、S2? |
| B、室温时,c(H+)=1×10-13mol/L的溶液中可能大量存在Mg2+、Cu2+、SO42-、NO3- |
| C、0.1mol/LNH4HCO3溶液中可能大量存在K+、Na+、NO3-、Cl- |
| D、中性溶液中可能大量存在Na+、Ca2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、还原剂是HCl,氧化剂是MnO2 |
| B、每生成1molCl2,转移电子的物质的量为2mol |
| C、每消耗1mol MnO2,起还原剂作用的HCl消耗2mol |
| D、标准状况下生成11.2L Cl2,转移电子的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
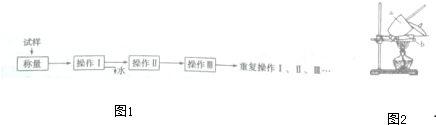
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、多孔电极a是燃料电池的负极 |
| B、生成的水从B口流出,汽油从C口流入 |
| C、在固体电解质中,O2-由正极移向负极 |
| D、通入汽油的一极是负极,电极反应为:C2H6+7O2--14e-═2CO2+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com