
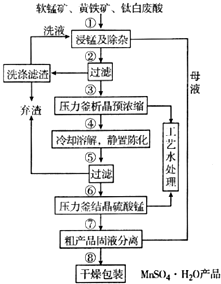
 随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:
随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题: (3)经查阅资料,生成相应氢氧化物时的pH如表所示.
(3)经查阅资料,生成相应氢氧化物时的pH如表所示.| 化学式 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
分析 (1)依据过滤装置和操作步骤选择玻璃仪器;
(2)根据“浸锰”温度与MnS2O6 的生成率的关系图进行解答,当温度150℃以上时,MnS2O6 的生成率几乎为0;
(3)根据表中氢氧化物的pH进行分析解答,调pH为3.5时只有Fe(OH)3开始沉淀,所以沉淀的主要成分是Fe(OH)3;二氧化锰有氧化性,能氧化二价铁离子和二氧化硫,所以①中加入一定量纯MnO2粉末,能将Fe2+氧化为Fe3+,将过量的SO2氧化除去;
(4)根据平衡移动的原理,当生成物的浓度减少时,平衡向正反应方向移动,CuS比MnS更难溶,MnS不断溶解生成更难溶的CuS;
(5)沉淀会附着SO42-离子,取最后一次洗涤液,用酸化的BaCl2溶液检验是否含有SO42-.
解答 解:(1)实验室在过滤操作过程中,使用的玻璃仪器名称为烧杯、玻璃棒、漏斗,
故答案为:烧杯、玻璃棒、漏斗;
(2)根据“浸锰”温度与MnS2O6 的生成率的关系图,当温度150℃以上时,MnS2O6 的生成率几乎为0,所以为减少MnS2O6 的生成,“浸锰”的适宜温度是150℃(或150℃以上),
故答案为:150℃(或150℃以上);
(3)查阅表调pH为3.5时只有Fe(OH)3开始沉淀,所以沉淀的主要成分是Fe(OH)3;二氧化锰有氧化性,能氧化二价铁离子和二氧化硫,所以①中加入一定量纯MnO2粉末,能将Fe2+氧化为Fe3+,将过量的SO2氧化除去,反应的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,MnO2+SO2=Mn2++SO42-,
故答案为:将Fe2+氧化为Fe3+,将过量的SO2氧化除去;Fe(OH)3;
(4)③中所得的滤液中含有Cu2+,添加过量的难溶电解质MnS,CuS比MnS更难溶,所以MnS不断溶解,
MnS(S)?Mn2+(aq)+S2-(aq);S2-(aq)+Cu2+(aq)?CuS(S)平衡右移,使Cu2+除去,
故答案为:MnS存在沉淀溶解平衡,MnS(S)?Mn2+(aq)+S2-(aq),加入后铜离子和硫离子结合市场难溶的硫化铜沉淀,S2-(aq)+Cu2+(aq)?CuS(S) 生成的CuS比MnS更难溶,促进MnS不断溶解,平衡右移,使Cu2+除去;
(5)沉淀会附着SO42-离子,取最后一次洗涤液,滴加酸化的BaCl2溶液,无沉淀生成,说明已洗净,反之硫酸根离子和钡离子结合生成硫酸钡沉淀,表明未洗干净,有SO42-;
故答案为:取少量最后一次洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净;反之则未洗干净.
点评 本题主要考查了制备高纯碳酸锰实验方案,读懂工艺流程图,掌握平衡移动原理、理解离子反应的本质是解答的关键,本题实验综合性强,题目难度中等.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:选择题
| 测定时刻/s | t1 | t2 | t3 | t4 |
| c(A)/mol•L-1 | 6 | 3 | 2 | 2 |
| c(B)/mol•L-1 | 5 | 3.5 | 3 | 3 |
| c(C)/mol•L-1 | 1 | 2.5 | 3 | 3 |
| A. | 在容器中发生的反应为2A+B?2C | |
| B. | 该温度下,此反应的平衡常数为0.25 | |
| C. | A的平衡转化率比B的平衡转化率低 | |
| D. | 起始加入的A、B物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1 367.0 kJ•mol-1(燃烧热) | |
| B. | KOH(aq)+HNO3(aq)═KNO3+H2O(l)△H=+57.3 kJ•mol-1(中和热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1(反应热) | |
| D. | 2NO2═O2+2NO△H=+116.2 kJ•mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +Br2→
+Br2→ ,反应类型是加成反应.
,反应类型是加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电作用力形成的化学键,叫离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中不一定含有金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使酸性高锰酸钾溶液褪色 | |
| B. | SO2使滴有酚酞的氢氧化钠溶液褪色 | |
| C. | SO2使品红溶液褪色 | |
| D. | SO2使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应时负极附近pH增大 | B. | 电池总反应为2H2+O2=2H2O | ||
| C. | O2在正极发生还原反应 | D. | 工作时OH-向负极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com