
| A. | 在共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电作用力形成的化学键,叫离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中不一定含有金属元素 |
分析 A.含离子键的化合物一定为离子化合物;
B.阴阳离子之间以静电作用成键;
C.离子化合物中可以含共价键;
D.非金属元素之间也能形成离子键.
解答 解:A.含离子键的化合物一定为离子化合物,则在共价化合物中不可能含有离子键,故A正确;
B.阴阳离子之间以静电作用成键,则阴阳离子之间通过静电作用力形成的化学键,叫离子键,故B正确;
C.离子化合物中可以含共价键,如NaOH中含共价键,为离子化合物,故C错误;
D.非金属元素之间也能形成离子键,如铵盐是由非金属元素形成的离子化合物,故D正确;
故选C.
点评 本题考查化学键和化合物的类型,注意离子键、共价键与化合物的关系,学会利用实例分析解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
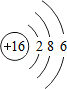 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
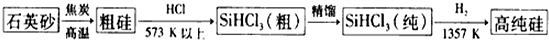
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
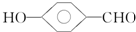 的沸点比
的沸点比 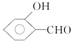 高,原因是
高,原因是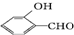 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
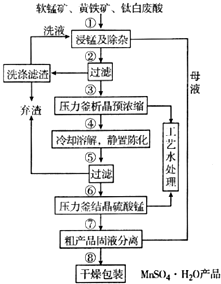 随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:
随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题: (3)经查阅资料,生成相应氢氧化物时的pH如表所示.
(3)经查阅资料,生成相应氢氧化物时的pH如表所示.| 化学式 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
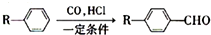 为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径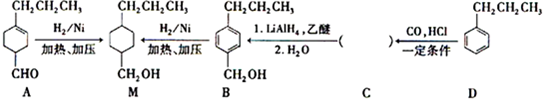
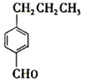 ,由C→B反应类型为加成反应.
,由C→B反应类型为加成反应.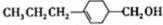 和
和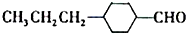 (写结构简式)两种互为同分异构体杂质生成.
(写结构简式)两种互为同分异构体杂质生成.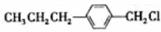 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$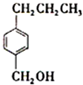 +NaCl;
+NaCl; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液化石油气、汽油、柴油和润滑油的主要成分都是碳氢化合物 | |
| B. | 可以通过灼烧时的特殊气味来鉴别蛋白质 | |
| C. | 用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯 | |
| D. | 乙烯、氯乙烯和聚氯乙烯都能因发生加成反应而使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质遇浓硝酸呈现黄色 | |
| B. | 淀粉溶液遇单质碘呈现蓝色 | |
| C. | 苯酚显弱酸性,其溶液可以使石蕊试液变红色 | |
| D. | 苯酚在空气中氧化呈现粉红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
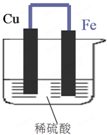 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com