
【题目】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: .
(2)已知化学键的键能为:
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | 391 | 945 |
又知反应N2(g)+3H2(g)2NH3(g)△H=a kJmol﹣1 . 试根据表中所列键能数据估算a的值为 .
(3)已知:C(s,石墨)+O2(g)═CO2(g)△H=﹣393kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2599kJmol﹣1
根据盖斯定律,计算 298K时C(s,石墨)和H2(g)反应生成1mol C2H2(g)的焓变为 .
【答案】
(1)2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=﹣1452.8kJ/mol
(2)﹣93
(3)+227.7kJ/mol
【解析】解:(1)5gCH3OH在氧气中燃烧生成CO2和液态水,放出113.5kJ热量,64g即1molCH3OH在氧气中燃烧生成CO2和液态水,放出1452.8kJ热量,则热化学方程式为:2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1452.8KJ/,所以答案是:2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1452.8KJ/mol;(2)N2(g)+3H2(g)2NH3(g)△H=945kJmol﹣1+436kJmol﹣1×3﹣391kJmol﹣1×6=﹣93kJmol﹣1=a kJmol﹣1 , 因此a=﹣93,所以答案是:﹣93;(3)已知:①C (s,石墨)+O2(g)=CO2(g)△H1=﹣393kJmol﹣1;②2H2(g)+O2(g)=2H2O (l)△H2=﹣571.6kJmol﹣1;③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=﹣2599kJmol﹣1; 2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②× ![]() ﹣③×
﹣③× ![]() 得到,所以反应焓变△H=2×(﹣393kJmol﹣1)+(﹣571.6kJmol﹣1)×
得到,所以反应焓变△H=2×(﹣393kJmol﹣1)+(﹣571.6kJmol﹣1)× ![]() ﹣(﹣2599kJmol﹣1)×
﹣(﹣2599kJmol﹣1)× ![]() =+227.7kJmol﹣1 , 所以答案是:+227.7kJmol﹣1;
=+227.7kJmol﹣1 , 所以答案是:+227.7kJmol﹣1;
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列离子能大量共存的一组是: ( )
A. Na+、 Pb2+、 SO42-、 Cl- B. Mg2+、 CO32-、 Cl-、 NO3-
C. Mg2+、 SO42-、 K+、 NH4+ D. Ca2+、 OH-、 Ba2+、 NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于四个图象的说法正确的是( ) 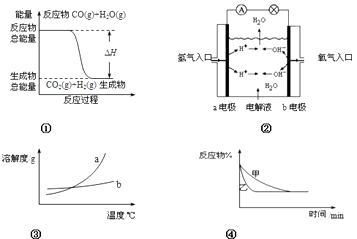
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H>0
B.图②为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯a
D.图④可以表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,且乙的压强大
3C(g)+D(s)的影响,且乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
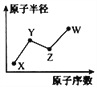
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___,说明理由__________________________________。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________。(写出有关反应的化学方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了从海带浸取液中提取碘,某同学设计了如下实验方案:( )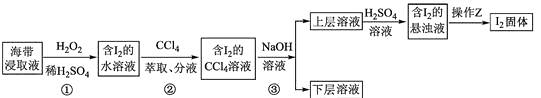
下列说法正确的是
A.①中反应的离子方程式:2I + H2O2 = I2 + 2OH
B.②中分液时含I2的CCl4溶液从分液漏斗上口倒出
C.③中得到的上层溶液中含有I
D.操作Z的名称是加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.三氧化二铁可以用来制作油漆
B.可用超纯硅制造的单晶硅来制造计算机的芯片
C.实验室用二氧化锰和浓盐酸共热制取少量氯气
D.氢氧化钠溶液要盛放在磨口玻璃塞的试剂瓶里
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2(g)+3H2(g)2NH3(g)在密闭容器中进行.下列关于该反应的说法正确的是( )
A.加热能减慢反应速率
B.增大压强能加快反应速率
C.反应达到平衡时,v(正反应)=v(逆反应)=0
D.反应达到平衡时,N2转化率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:M+N﹣→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到30℃时,完成反应的10%需要的时间为( )
A.9 min
B.27 min
C.13.5 min
D.3 min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂。有研究表明,H2O2溶液的漂白性是HO2—所致。
(1)H2O2溶液显弱酸性,测得0.15 mol·L1 H2O2溶液pH约为6。写出H2O2生成HO2—的电离方程式:。
(2)其他条件相同时,研究不同初始pH条件下H2O2溶液的漂白效果,结果如下: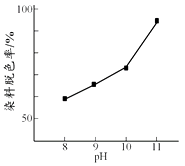
由上图可得到的结论是 , 结合平衡移动原理简述理由:。
(3)实验发现: 若pH >11,则H2O2溶液的漂白效果随pH增大而降低。针对这一现象,继续进行实验,发现溶液中H2O2的分解与pH有关。测定不同初始pH条件下,初始浓度均为0.15 mol·L1 的H2O2溶液发生分解反应,结果如下:
初始pH | pH = 10 | pH = 12 |
1小时后H2O2溶液浓度 | 0.13 mol·L1 | 0.07 mol·L1 |
1小时后pH | 没有明显变化 | 没有明显变化 |
查阅资料:HO2-+H2O2=H2O+O2+OH-。
①结合离子方程式解释1小时后pH没有明显变化的原因:。
②从反应速率的角度分析pH过大,H2O2溶液漂白效果会降低的原因:。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com