
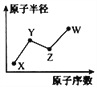
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___,说明理由__________________________________。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________。(写出有关反应的化学方程式)
【答案】 H N O Cl 否 HClO不是氯的最高价氧化物对应水化物,不能证明非金属性强弱。 HClO 浓硝酸分解产生的NO2溶于其中 C+4HNO3(浓)![]() 4NO2↑+CO2↑+2H2O 3NO2+H2O=2 HNO3 +NO (写出此反应即给分)( Ca(OH)2+2HNO3= Ca(NO3)2+2H2O )
4NO2↑+CO2↑+2H2O 3NO2+H2O=2 HNO3 +NO (写出此反应即给分)( Ca(OH)2+2HNO3= Ca(NO3)2+2H2O )
【解析】试题分析:W、X、Y、Z是四种常见的短周期主族元素。由图可知,X的原子序数和原子半径均最小,则X为H元素。Y、Z两种元素的单质是空气的主要成分,则Y是N元素、Z是O元素;W的半径大于Z,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W的最外层有7个电子,故W为第VIIA的Cl元素。
(1)X、Y、Z、W四种元素的元素符号分别为H、N、O、Cl;
(2)HNO3的酸性比HClO强,有人据此认为N的非金属性强于Cl,这种看法不正确,因为HClO不是氯的最高价氧化物对应水化物,不能证明其非金属性强弱。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,则甲为次氯酸,其化学式为HClO;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,则乙为硝酸,因为浓硝酸分解产生的NO2溶于其中而显黄色。把红热的木炭浓硝酸,该反应的化学方程式为C+4HNO3(浓)![]() 4NO2↑+CO2↑+2H2O,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是NO2与水反应生成硝酸,硝酸与石灰水反应生成硝酸钙,CO2不与硝酸钙反应,故不变浑浊。化学方程式为3NO2+H2O=2 HNO3+NO 、Ca(OH)2+2HNO3= Ca(NO3)2+2H2O。
4NO2↑+CO2↑+2H2O,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是NO2与水反应生成硝酸,硝酸与石灰水反应生成硝酸钙,CO2不与硝酸钙反应,故不变浑浊。化学方程式为3NO2+H2O=2 HNO3+NO 、Ca(OH)2+2HNO3= Ca(NO3)2+2H2O。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是
4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是
A. v(C)=0.2mol(L·s) B. v(D)=6mol (L·min)
C. V(A)=4mol(L·min) D. v(B)=8mol(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 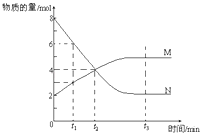
A.反应的化学方程式为:2 NM
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是
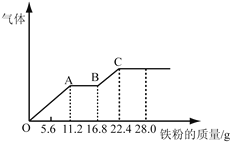
A. 混合酸中HNO3物质的量浓度为2mol/L
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 原混合酸中H2SO4物质的量为0.4 mol
D. 第二份溶液中最终溶质为FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)═CH3OCH3(g)+H2O(g)
下列说法正确的是( )
容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A.该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: .
(2)已知化学键的键能为:
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | 391 | 945 |
又知反应N2(g)+3H2(g)2NH3(g)△H=a kJmol﹣1 . 试根据表中所列键能数据估算a的值为 .
(3)已知:C(s,石墨)+O2(g)═CO2(g)△H=﹣393kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2599kJmol﹣1
根据盖斯定律,计算 298K时C(s,石墨)和H2(g)反应生成1mol C2H2(g)的焓变为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于硫化氢气体在空气中完全燃烧的产物,下列叙述正确的是
①具有臭鸡蛋气味的气体 ②是淡黄色的固体
③是无色有刺激性气味的气体 ④是造成酸雨的主要物质
A.②B.③C.①④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中不能用化合反应的方法制得的是( )
①SiO2 ②H2SiO3 ③Fe(OH)3 ④Al(OH)3 ⑤FeCl2 ⑥CaSiO3
A. ①③ B. ②④
C. ②③④⑤ D. ②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com