
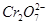 和
和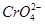 ,常用的方法有两种。
,常用的方法有两种。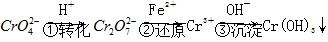 。
。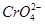 (黄色)+2H+
(黄色)+2H+
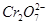 (橙色)+H2O。
(橙色)+H2O。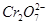 ,需要________mol的FeSO4·7H2O。
,需要________mol的FeSO4·7H2O。 Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________________。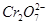 的废水,电解时阳极反应式为________,阴极反应式为________,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是________________________。
的废水,电解时阳极反应式为________,阴极反应式为________,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是________________________。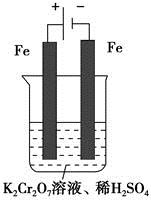
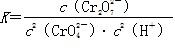 (2)AC (3)0.6
(2)AC (3)0.6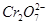 )/[c2(
)/[c2(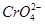 )·c2(H+)]。(2)由反应①可知,平衡发生移动,溶液的pH发生变化,故pH不变时说明反应达到平衡,A项正确;
)·c2(H+)]。(2)由反应①可知,平衡发生移动,溶液的pH发生变化,故pH不变时说明反应达到平衡,A项正确;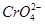 和
和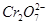 中Cr均为+6价,该反应不是氧化还原反应,B项错误;在酸性环境中,溶液中c(
中Cr均为+6价,该反应不是氧化还原反应,B项错误;在酸性环境中,溶液中c(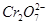 )较大,溶液呈橙色,C项正确。(3)在第②步反应中
)较大,溶液呈橙色,C项正确。(3)在第②步反应中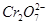 被还原为Cr3+,0.1 mol
被还原为Cr3+,0.1 mol 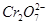 被还原时转移电子的物质的量为0.1 mol×2×(6-3)=0.6 mol,而还原剂Fe2+被氧化为Fe3+,故需要消耗0.6 mol FeSO4·7H2O。(4)在第②步反应中Fe2+被氧化为Fe3+,故第③步还有Fe(OH)3生成。(5)电解池的阳极发生氧化反应,Fe作阳极,则Fe电极本身被氧化,故阳极反应式为Fe-2e-=Fe2+;阴极则是电解质溶液中的H+得电子,发生还原反应生成氢气,故阴极反应式为2H++2e-=H2↑;阳极生成的金属阳离子移向阴极,而阴极反应消耗了H+,打破了水的电离平衡,促进了水的电离,使溶液中的OH-浓度增大,溶液逐渐呈碱性,从而使金属阳离子在阴极区形成沉淀。
被还原时转移电子的物质的量为0.1 mol×2×(6-3)=0.6 mol,而还原剂Fe2+被氧化为Fe3+,故需要消耗0.6 mol FeSO4·7H2O。(4)在第②步反应中Fe2+被氧化为Fe3+,故第③步还有Fe(OH)3生成。(5)电解池的阳极发生氧化反应,Fe作阳极,则Fe电极本身被氧化,故阳极反应式为Fe-2e-=Fe2+;阴极则是电解质溶液中的H+得电子,发生还原反应生成氢气,故阴极反应式为2H++2e-=H2↑;阳极生成的金属阳离子移向阴极,而阴极反应消耗了H+,打破了水的电离平衡,促进了水的电离,使溶液中的OH-浓度增大,溶液逐渐呈碱性,从而使金属阳离子在阴极区形成沉淀。

科目:高中化学 来源:不详 题型:单选题
 4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是 ( )
4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是 ( )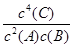
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示: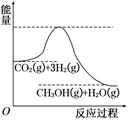
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量
2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量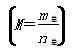 随温度(T)的变化曲线如图所示,下列说法正确的是( )
随温度(T)的变化曲线如图所示,下列说法正确的是( )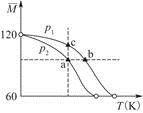
| A.该过程的ΔH<0 |
| B.气体压强:p(a)<p(b)=p(c) |
| C.平衡常数:K(a)=K(b)<K(c) |
| D.测定乙酸的相对分子质量要在高压、低温条件 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是 | A.2v(NH3)=v(CO2) |
| B.密闭容器中c(NH3)∶c(CO2)=2∶1 |
| C.密闭容器中混合气体的密度不变 |
| D.密闭容器中氨气的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表: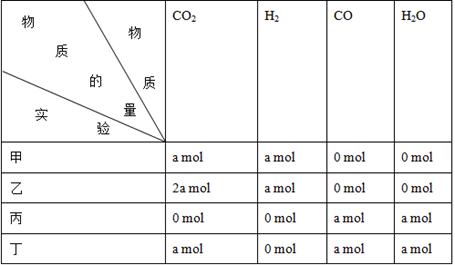
| A.乙=丁>丙=甲 | B.乙>丁>甲>丙 |
| C.丁>乙>丙=甲 | D.丁>丙>乙>甲 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
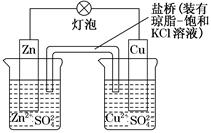
| A.正极反应为:Zn―→Zn2++2e- |
| B.电池反应为:Zn+Cu2+=Zn2++Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3Z(g) △H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) △H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是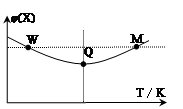
| A.升高温度,平衡常数增大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.Q点时,Y的转化率最大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO2(正反应为放热反应),不能说明已经达到平衡状态的是( )
2NO2(正反应为放热反应),不能说明已经达到平衡状态的是( )| A.正反应生成NO2的速率和逆反应生成O2的速率相等 |
| B.反应容器中压强不随时间的变化而变化 |
| C.混合气体颜色保持不变 |
| D.混合气体的平均相对分子质量不随时间变化而变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com