
(本题共8分)
某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量小于150,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1)A的分子式是 。
(2)若A能与NaHCO3溶液反应放出CO2气体,其结构可能有 种。
(3)若A与NaOH溶液在加热时才能较快反应,且1molA消耗1mol NaOH,则A的所有可能的结构简式是 。
(4)若A与NaOH溶液在加热时才能较快反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有 种,其中不能发生银镜反应的物质的结构简式是: 。
(1)C8H8O2 (2)4 (2分)
(3)

(4)4  (2分)
(2分)
【解析】(1)氧元素的质量分数为23.5%,因为 ,所以分子中最多含有
,所以分子中最多含有
2个氧原子。如果含有1个则相对分子质量是 ,而苯环的相对分子质量一定是
,而苯环的相对分子质量一定是
大于68的,所以只能是含有2个氧原子,则其相对分子质量是 ,因此碳、氢
,因此碳、氢
原子数分别是 ,所以分子式为C8H8O2
。
,所以分子式为C8H8O2
。
(2)若A能与NaHCO3溶液反应放出CO2气体,则含有羧基,则可以是苯乙酸或甲基苯甲酸(含邻、间、对),因此共计是四种。
(3)若A与NaOH溶液在加热时才能较快反应,且1molA消耗1mol NaOH,则分子中应该含有酯基,所以结构简式为
 。
。
(4)若A与NaOH溶液在加热时才能较快反应,且1mol A消耗2mol NaOH,则分子中应该含有酯基,且水解后又产生1个酚羟基,因此可以是甲酸形成的酯,而甲基的位置可以是邻、间、对,或者是乙酸形成的酯,其结构简式为 ,因此共计是4种。
,因此共计是4种。


科目:高中化学 来源:2012届上海市松江区高三上学期期末(1月)考试化学试卷(带解析) 题型:填空题
(本题共8分)
已知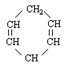 可简写为
可简写为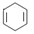 。现有某化合物W的分子结构可表示为
。现有某化合物W的分子结构可表示为 。根据题意回答:
。根据题意回答:
1.W属于
A.芳香烃 B.环烃 C.不饱和烃 D.炔烃
2.W的分子式为 ,它的一氯代物有 种。
3.有关W的说法错误的是
A.能发生还原反应 B.能发生氧化反应
C.易溶于水 D.等质量的W与苯分别完全燃烧,前者消耗的氧气多
4.W有一种芳香族的同分异构体,该物质能在一定条件下发生聚合反应,相应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2012届三校上海市(复旦、交大、华师大二附中)高三联考化学试卷(带解析) 题型:填空题
(本题共8分)
某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量小于150,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1)A的分子式是 。
(2)若A能与NaHCO3溶液反应放出CO2气体,其结构可能有 种。
(3)若A与NaOH溶液在加热时才能较快反应,且1molA消耗1mol NaOH,则A的所有可能的结构简式是 。
(4)若A与NaOH溶液在加热时才能较快反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有 种,其中不能发生银镜反应的物质的结构简式是: 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省高三开学考试化学试卷(解析版) 题型:实验题
(本题共16分)某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
[实验设计]
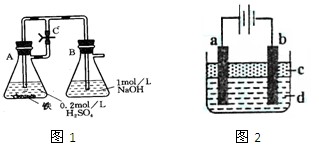
方法一:按照图1进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行。最终在_______容器中观察到白色沉淀,该实验中涉及到的化学方程式有: 。
方法二:按图2进行实验,最终在两极间的溶液中首先观察到白色沉淀。请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl2溶液 ⑥乙醇 ⑦Fe棒 ⑧植物油 ⑨碳棒
a为___________,b为___________,c为___________,d为___________。(填序号)
[探究思考]实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
|
资料名称 |
物理性质描述 |
化学性质描述 |
|
《化学辞典》,顾翼东编,1989年版P637 |
白色无定形粉末或白色至淡绿色六方晶体 |
与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
|
《大学普通化学(下册)》傅鹰著P637 |
白色沉淀 |
此沉淀易被氧化成微绿色Fe3(OH)8 |
|
《普通化学教程》(下册)P788 |
白色 |
能强烈吸收O2,迅速变成棕色Fe(OH)3。这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+。 |
阅读该资料后,你对上述实验中出现灰绿色或绿色的现象的解释是:__________ ;资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成__________________。
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2·nH2O所致。用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势。
加热时,“方法一”中弹簧夹C应处于___________(填“打开”或“关闭”)状态,容器A中的反应须处于___________(填“停止”或“发生”)状态。写出该实验中支持乙同学观点的化学方程式_______________。
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路。 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市普陀区高三4月质量调研(二模)化学试卷(解析版) 题型:填空题
(本题共8分)在玻璃生产中,熔炉里原料发生的主要反应为:
2Na2CO3+CaCO3+3SiO2 2Na2SiO3+CaSiO3+3CO2↑
2Na2SiO3+CaSiO3+3CO2↑
(1).某反应物在熔融状态下不导电,它属于_____晶体。
(2).上述反应里,在周期表中相邻两元素的原子半径______>______(填元素符号) ,处于同一周期元素的名称是__________________。
(3).上述反应里金属性最强的短周期元素,其原子核外有______种不同能级的电子,其单质在O2中充分燃烧, 产物的电子式为_____________。
(4).H2与O2发生反应的过程用模型图示如下(“—”表示化学键):

其中过程Ⅰ是______过程(填“吸热”、“放热”或“没有能量变化”)。图④中产生了由极性键构成的__________分子(填“极性”或“非极性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com