
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
| 2 |
| 3 |
| 2 |
| 3 |
| 0.04mol |
| 0.1L |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
| A、①②③④ | B、⑥⑦ |
| C、①③⑤ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、因为水分子间的氢键,H2O比H2S稳定 | ||||||
| B、氯水、氨水、王水是混合物,水银、水玻璃是纯净物 | ||||||
| C、HCl、NH3、BaSO4是电解质,CO2、Cl2、CH3CH2OH是非电解质 | ||||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体能产生丁达尔现象 |
| B、Fe(OH)3胶体是均一的分散系 |
| C、Fe(OH)3胶体的分散质能透过滤纸 |
| D、Fe(OH)3胶体中分散质粒子的大小在1-100纳米之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、和浓硫酸共热至170℃乙醚时,键②断裂 |
| D、在铜催化下和氧气反应时,键①和③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L己烷中共价键数目为19NA |
| B、1L 1mol/L FeCl3溶液中含有NA个Fe3+ |
| C、足量Cl2与5.6g Fe完全反应时,转移的电子数为0.2NA |
| D、由CO2和O2组成的混合物中共有NA个分子,其中氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
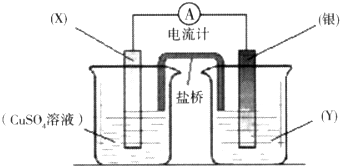
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com