
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钠溶液中得到氯化钠固体,选择装置________(填代表装置图的字母,下同);
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为(两个)_______。
(3)装置A中①的名称是________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO![]() 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液
④加入适量盐酸 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
【答案】 D B 萃取、分液 冷凝管 AD
【解析】(1)蒸发可以实现易溶于水的固体和水的分离,从氯化钠溶液中得到氯化钠固体可用蒸发,选择装置为D;
(2)从碘水中分离出I2,选择装置B,该分离方法的名称为萃取、分液;
(3)装置A中①的名称是冷凝管;
(4)除去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42-时,先加水溶解,所以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3↓,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,然后过滤,最后调节溶液的pH等于7后蒸发即可,所以其顺序是⑤③②①⑥④⑦或⑤②③①⑥④⑦,故答案为AD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列过程可发生酯化反应的是( )
A. 光照条件下CH4与Cl2混合
B. 乙烯通入溴的CCl4溶液中
C. 苯与浓硫酸和浓硝酸混合加热
D. 乙醇和冰醋酸与浓硫酸混合加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法正确的是( )

A. 该混合气体中一定含有乙烯
B. 该混合气体一定含有甲烷和乙炔
C. 在110℃条件下,混合气体与氧气混合,总混合气燃烧前后体积不变
D. 若混合气体由CH4和C2H4组成,则其体积比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大。在下图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物。常温时,0.1mol·L-1的a溶液的pH为1, d为红棕色气体,e为无色气体。下列说法正确的是

A. 元素的非金属性:Y>Z>X
B. 反应①中消耗lmola时转移电子数与反应②中生成1mol a时转移电子数相等
C. 原子半径的大小:Y<Z<W
D. Y的氢化物常温常压下为气态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是

A. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l:2
B. 石墨l极发生的电极反应为2CH3OH+CO-e-=(CH3O)2CO+H+
C. 石墨2极与直流电源正极相连
D. H+由石墨2极通过质子交换膜向石墨l极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合化学与环境相关知识,下列有关说法正确的是
A.SO2、NO2、CO2均属于大气污染物
B.酸雨是pH小于5.6的降水
C.CO2也会导致酸雨的形成
D.大气中O2含量的增加会导致温室效应加剧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图2中的物质补充到图1中,可得到一个完整的氧化还原反应离子方程式(未配平)。

对该氧化还原反应的离子方程式,说法不正确的是
A.![]() 作氧化剂,具有氧化性
作氧化剂,具有氧化性
B.氧化性:![]() >
>![]()
C.氧化剂和还原剂的物质的量之比为5∶2
D.若有2 mol Mn2+参加反应,则转移10 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g) + H2O(g)==CO(g)+3H2(g) △H1
已知:
①CH4、H2、CO 的燃烧热(△H)分别为-a kJmol-1、-b kJmol-1、-c kJmol-1;
②H2O(l) =H2O(g) △H=+dkJmol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJmol-1。
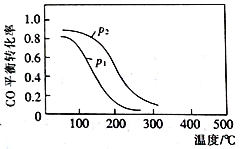
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________(填“>”“<”或“ = ”)0。
②写出两条可同时提高反应速率和CO转化率的措施:________________________ 。
③下列说法正确的是____________(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
C.容器内气体压强不再变化时,反应达到最大限度
D.图中压强p12
④03 min内用CH3OH表示的反应速率v(CH3OH)=_________mol L-1·min-1。
⑤200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com