
����Ŀ���� X��Y��Z ����Ԫ�أ�X ���л��������бغ���Ԫ�أ� Y �ǵؿ��ﺬ������Ԫ�أ�Z ���� �������Ԫ�ء�X��Y��Z ����Ԫ����ɵ��л��� M �ܱ����Ը�������������� N��Ϊ�˲ⶨ�л��� M �Ľṹ��������ʵ�飺
���� 4.6 g �л��� M ��ȫȼ�գ�������� 0.2mol CO2 �� 5.4 g ˮ�� ���������Ǽ���л��� M���õ���ͼ 1 ��ʾ������ͼ�� ���ú˴Ź����Ǵ����л��� M���õ���ͼ 2 ��ʾͼ�ס�
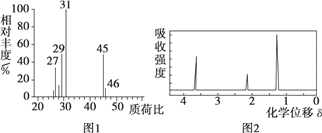
�Իش��������⣺
��1��M �Ľṹ��ʽ��___________________��N �к��еĹ����ŵĽṹ��ʽΪ_____________��
��2��д�� M ��ͭ�������Ҽ���������������������Ӧ�Ļ�ѧ����ʽ___________________��
��3��д�� M �� N ��Ũ H2SO4���������·�����Ӧ�Ļ�ѧ����ʽ___________________��
���𰸡� CH3CH2OH ��COOH 2CH3CH2OH��O2![]() 2CH3CHO��2H2O CH3COOH��CH3 CH2OH
2CH3CHO��2H2O CH3COOH��CH3 CH2OH![]() CH3COOCH2CH3��H2O
CH3COOCH2CH3��H2O
��������X��Y��Z ����Ԫ�أ�X���л��������бغ���Ԫ�أ���XΪ̼Ԫ�أ�Y�ǵؿ��ﺬ������Ԫ�أ���YΪ��Ԫ�أ�Z �����������Ԫ�أ���ZΪ��Ԫ�ء�
�������Ǽ���л��� M���õ���ͼ 1 ��ʾ������ͼ������Է�������Ϊ46��ͨ�����㣬������̼�����ʵ���Ϊ0.2mol��ˮ�����ʵ���Ϊ![]() =0.3mol�������л����к���ԭ�ӵ����ʵ���=
=0.3mol�������л����к���ԭ�ӵ����ʵ���=![]() =0.1mol������̼������ԭ�Ӹ�����Ϊ2:6:1��������Է���������������ѧʽΪC2H6O�����ݺ˴Ź�������������������ԭ�ӣ�����Ϊ3:2:1������M�Ľṹ��ʽΪ��CH3CH2OH��M �ܱ����Ը�������������� N��NΪCH3COOH����1��M �Ľṹ��ʽ��CH3CH2OH��N ΪCH3COOH�����еĹ����ŵĽṹ��ʽΪ-COOH����2��CH3CH2OH��ͭ�������Ҽ���������������������Ӧ����CH3CHO����Ӧ�Ļ�ѧ����ʽΪ��2CH3CH2OH��O2
=0.1mol������̼������ԭ�Ӹ�����Ϊ2:6:1��������Է���������������ѧʽΪC2H6O�����ݺ˴Ź�������������������ԭ�ӣ�����Ϊ3:2:1������M�Ľṹ��ʽΪ��CH3CH2OH��M �ܱ����Ը�������������� N��NΪCH3COOH����1��M �Ľṹ��ʽ��CH3CH2OH��N ΪCH3COOH�����еĹ����ŵĽṹ��ʽΪ-COOH����2��CH3CH2OH��ͭ�������Ҽ���������������������Ӧ����CH3CHO����Ӧ�Ļ�ѧ����ʽΪ��2CH3CH2OH��O2![]() 2CH3CHO��2H2O����3��CH3CH2OH �� CH3COOH��Ũ H2SO4���������·�����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH��CH3 CH2OH
2CH3CHO��2H2O����3��CH3CH2OH �� CH3COOH��Ũ H2SO4���������·�����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH��CH3 CH2OH![]() CH3COOCH2CH3��H2O��
CH3COOCH2CH3��H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ����ȷ���ǣ�������
A.Na2CO3����
B.NaHSO4�� ��
C.NaOH����
D.HCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000mol/L NaOH��Һ�ζ� 20.00mL 0.1000 mol/L
CH3COOH��Һ�ζ���������ͼ������˵����ȷ����

A. ������ʾ��Һ�У�c(CH3COO-)+ c(OH-) ��c(CH3COOH)+ c(H+)
B. ������ʾ��Һ�У�c(Na+) ��c(CH3COOH)+ c(CH3COO-)
C. ������ʾ��Һ�У�c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
D. �ζ������п��ܳ��֣�c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵������ȷ���ǣ� ��
A. ����Ũ���ᡢŨ���Ṳ�Ȳ����� 70��80 ����Ӧ����������
B. �ڼױ��м����������Ը��������Һ������ɫ����ȷ�Ľ��������ڱ����Բ�����Ӱ�죬ʹ�����ױ�����
C. ���ױ������ϵ�һ����ԭ�ӱ�һ���� 3 ��̼ԭ�ӵ����ȡ�������ò����� 6 ��
D. �ƵĽṹ��ʽΪ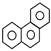 ���������ᷴӦ�������� 5 ��һ����ȡ����
���������ᷴӦ�������� 5 ��һ����ȡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ��������������� ��
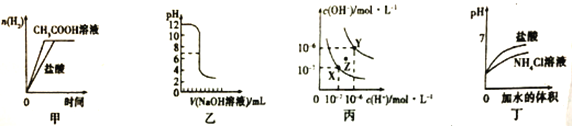
A. ��ͼ���߱�ʾ�������������ʵ���Ũ�ȵ�����ʹ�����Һ�зֱ��������þ�۲���H2�����ʵ����ı仯
B. ��ͼ��ʾ��0.01mol/L��NaOH��Һ���뵽ϡ�����еĵζ�����
C. ��ͼΪˮ�ĵ������ߣ���Z�㵽X�㣬�ɲ�����ˮ�м�������NaOH����ķ���
D. ��ͼ�����߱�ʾ��pH��ͬ��NH4Cl��Һ������ϡ����ͬ����ʱ������pH�ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������塷�жԾ���â��������������������������ˮ��֭�����壬�پ��������룬��ľ���У����ޣ����â�������ߡ�������û���漰�IJ��������ǣ�������
A.�ܽ�B.����C.��ȡD.��ȴ�ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Լ���ơ������Լ��������л�±���������þ����ˮ���ѻ������(THF)�з�Ӧ�Ƶã����л��ϳ�����;�㷺����Ӧԭ�����£�
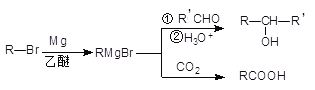
��A( ![]() )�ϳ� I (
)�ϳ� I ( ![]() )������ͼ��
)������ͼ��
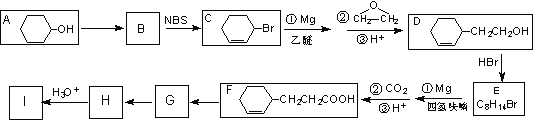
����֪��NBSΪ�廯�Լ�����һ������������ϩ�������������ϩ������
(1) ����A������Ϊ_________________����A����B�ķ�Ӧ������_________��
(2) д����A�Ʊ� ![]() �Ļ�ѧ����ʽ_________________________��
�Ļ�ѧ����ʽ_________________________��
(3) �������һ���������ܼ��������( ![]() )����õ���������Ľṹ��ʽΪ_____________________��
)����õ���������Ľṹ��ʽΪ_____________________��
(4) д����G����H�Ļ�ѧ����ʽ_____________________________________��
(5) д����������Ҫ���I��ͬ���칹��Ľṹ��ʽ_____________________��(д��һ�ּ��ɣ�ͬһ̼�ϲ�������2���ǻ�)
�� �����廯���� �� ��Ԫ�� �� ��������5�ֻ�ѧ������H
(6) ����������Ϣ����A��A�ƵõĻ���ͪ( ![]() )Ϊԭ�Ϻϳ�
)Ϊԭ�Ϻϳ�![]() ��
��![]() ��______________________��
��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ka1(H2C2O4)��10��1.3�� Ka2(H2C2O4)��10��4.2����0.1000 mol��L��1 NaOH��Һ�ζ�10.00 mL 0.1000 mol��L��1 H2C2O4��Һ���õζ���������ͼ������˵����ȷ����
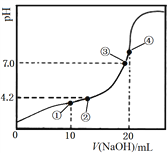
A. �����ʾ��Һ�У�c(Na+)>c(HC2O4��)��c(H2C2O4)��c(C2O42��)
B. �����ʾ��Һ����c(HC2O4��)��c(C2O42��)
C. �����ʾ��Һ����c(Na+)��c(HC2O4��) + c(C2O42��)
D. �����ʾ��Һ����c(Na+) + 2c(H2C2O4) + 2c(H+)��2c(OH��) + 2c(C2O42��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����¶��£���һ�����������͵����Ļ����������ѹ�ܱ������н��з�Ӧ���ﵽƽ��ʱά���¶Ȳ��䣬��û��������ܶ��Ƿ�Ӧǰ�ܶȵ�1.25������ﵽƽ��ʱ���������������Ϊ
A. 25% B. 27.5 % C. 30% D. 37.5%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com