
【题目】下列有关说法不正确的是( )
A. 苯与浓硝酸、浓硫酸共热并保持 70~80 ℃反应生成硝基苯
B. 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于苯环对侧链的影响,使侧链易被氧化
C. 若甲苯苯环上的一个氢原子被一个含 3 个碳原子的烷基取代,所得产物有 6 种
D. 菲的结构简式为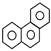 ,它与硝酸反应,可生成 5 种一硝基取代物
,它与硝酸反应,可生成 5 种一硝基取代物
科目:高中化学 来源: 题型:
【题目】已知:4FeO42-+10H2O=4Fe(OH)3↓+8OH-+3O2↑ ,测得c(FeO42-)在不同条件下变化如图甲、乙、丙、丁所示:

下列说法正确的是
A. 图甲表明,其他条件相同时,温度越低FeO42-转化速率越快
B. 图乙表明,其他条件相同时,碱性越强FeO42-转化速率越快
C. 图丙表明,其他条件相同时,钠盐都是FeO42-优良的稳定剂
D. 图丁表明,其他条件相同时,碱性条件下Fe3+能加快FeO42-的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3===K2O+5Na2O+16N2↑下列说法正确的是:
A. KNO3是还原剂,其中氮元素被氧化
B. 生成物中的N2是氧化产物,K2O是还原产物
C. 每转移1 mol电子,可生成标准状况下N2的体积为35.84 L
D. 若有65 g NaN3参加反应,则被氧化的N的物质的量为3.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项说法正确的是( )
A.白磷应放在冷水中保存
B.将水注入浓硫酸中以稀释浓硫酸
C.硝酸银放在无色试剂瓶中保存
D.在蒸发皿中加热分解氯酸钾固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十氢奈是具有高储氢密度的氢能载体,经历“十氢奈(C10H18 )→四氢奈(C10H12)→奈(C10H8)”的脱氢过程释放氢气。已知:
C10H18(l)![]() C10H12(l)+3H2(g) △H1
C10H12(l)+3H2(g) △H1
C10H12(l)![]() C10H8(l)+2H2(g) △H2
C10H8(l)+2H2(g) △H2
△H1>△H2>0;C10H18→C10H12的活化能为Ea1,C10H12→C10H8的活化能为Ea2,十氢奈的常压沸点为192℃;在192℃,液态十氢奈的脱氢反应的平衡转化率约为9%。请回答:
(1)每1mol 十氢萘液体可储存5mol氢气,可运载到使用氢气的场所,在催化剂的作用下释放氢气,生成的液体萘可重复催化加氢来储存氢气,如图所示,则△H1+△H2=__________。
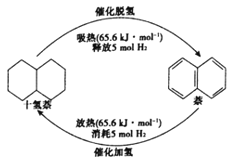
(2)有利于提高上述反应平衡转化率的条件是__________。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(3)不同压力和温度下十氢萘的平衡转化率如图所示,结合图示回答问题:
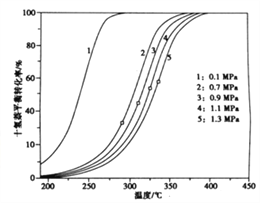
①在相同压强下升高温度,未达新平衡前,v正__________v逆(填写“大于”“小于”或“等于”)。
②研究表明,将适量的十氢奈置于恒容密闭反应器中,既升高温度又增大压强,十氢萘的转化率也升高,可能理由是______________________________________。
(4)温度335℃,在恒容密闭反应器中进行高压液态十氢奈(1.00 mol)催化脱氢实验,测得液态C10H12和液态C10H8的产率x1和x2(以物质的量分数计)随时间变化关系,如图所示。
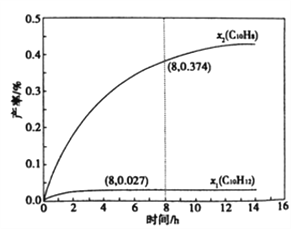
①在8h时,反应体系内氢气的量为_______mol(忽略其他副反应),液态十氢奈的转化率是____。
②x1显著低于x2的原因是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质 量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水; ②用质谱仪检测有机物 M,得到如图 1 所示的质谱图; ③用核磁共振仪处理有机物 M,得到如图 2 所示图谱。
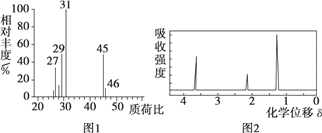
试回答下列问题:
(1)M 的结构简式是___________________,N 中含有的官能团的结构简式为_____________。
(2)写出 M 在铜作催化剂且加热条件下与氧气发生反应的化学方程式___________________。
(3)写出 M 与 N 在浓 H2SO4加热条件下发生反应的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又成丹砂”。这句话所指的是:①红色的硫化汞(即丹砂,化学式为HgS)在空气中灼烧有汞生成;②汞和硫在一起研磨生成黑色硫化汞;③黑色硫化汞隔绝空气加热变成红色硫化汞晶体。
(1)在上述三点含义中,描述的______(填“有”或“无”)物理变化,若有的话,请写出哪些?并说明理由______(填序号),理由是______。
(2)在上述三点含义中,描述的______(填“有”或“无”)化学变化,若有的话,请写出哪些?并写出反应的文字表达式:_______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式H++OH﹣=H2O表示的反应是( )
A.稀醋酸和氢氧化钾反应
B.硫酸氢钠和烧碱溶液反应
C.稀盐酸和氢氧化铜反应
D.稀硫酸和氢氧化钡溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com