
【题目】在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温度,下列说法正确的是
A.溶液中有晶体析出, Na+数目不变
B.溶液中的OH- 物质的量浓度不变,有O2放出
C.溶质的质量分数增大
D.溶液中NaOH的浓度减小,有O2放出
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是

A. 元素W的最高价氧化物对应水化物的酸性比Q的强
B. 离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+)
C. 元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D. X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有氧化镁、氧化铝的混合物完全溶于200 mL盐酸,而后逐滴加入1.0 mol·L-1的NaOH溶液。溶液中生成沉淀的物质的量随加入的NaOH的溶液体积的变化,如图所示。
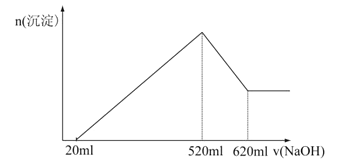
(1)试说明最初加入的20 mL NaOH溶液的作用。
(2)求所用盐酸的物质的量浓度。
(3)求氧化镁、氧化铝物质的量之比。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往100mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的CO2的体积(标准状况)与M的质量W的关系如图所示。请回答下列问题:

(1)b点时M的组成成分为__________.
(2)若要使b点生成的盐的质最变为8.4g,则应继续向溶液中通入二氧化碳________以标准状况下).
(3)若向生成的7.16g盐的溶液中加入一定量的某物质,充分反应后,减压低温蒸发得到纯净的碳酸钠固体(无结晶水)8.4g。
① 若只加入0.03mol某物质,则加入的物质可以是___________或____________;
② 若只加入0.06mol某物质,则加入的物质可以是________、_______或________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及6.00mol/L的硫酸,其他试剂任选。填写下列空白:

(1)B 中盛有一定量的NaOH溶液,A中应预先加入的试剂是___________,A中反应的离子方程式___________。
(2)实验开始时应先将活塞E_______________(城”打开”或“关闭”) ,其目的是_______________,在C中收集到的气体主要是_______________。
(3)简述生成Fe(0H)2的操作过程:_______________________。
(4)拔去装置B中的橡皮塞,让空气进入B中,可观察到的现象是_______________;写出有关反应的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. Si、Se、Ge都是重要的半导体材料 B. FeCl3溶液可用于制作印刷电路板
C. 溴元素又名海洋元素,可用于生产杀虫剂、熏蒸剂等 D. 硫酸铜溶液常用作游泳池及饮用水的消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液,①碘水中提取单质碘 ②碘和四氯化碳的混合物 ③汽油和氯化钠溶液,分离以上混合物的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com