
某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质.当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用.填空
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为 
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为 (已知该反应为置换反应).
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O,KClO4含有化学键的类型为 ,KCl在灼烧时得焰色为 色.
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为 .
(5)100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况).
①用碱石灰除去的物质为 ;
②该产气药剂中NaN3的质量分数为 .
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2017届江西省、宜春一中高三7月联考化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A. 用10 mL量筒量取7.13mL稀盐酸
B. 用托盘天平称量25.20g NaCl
C. 用广泛pH试纸测得某溶液的pH为2.3
D. 用25 mL滴定管做中和滴定时,用去某浓度的碱溶液21.70 mL
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的值。下列说法正确的是
A.2.4g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.8NA
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA
C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
D.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
查看答案和解析>>
科目:高中化学 来源:2017届湖南衡阳八中高三实验班暑期第一次月考理综化学(解析版) 题型:实验题
(本题满分18分)草酸亚铁为黄色固体,作为一种化工原料,可广泛用于涂料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:
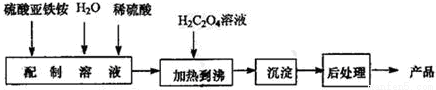
(1)配制(NH4)2Fe(SO4)2 6H2O溶液时,需加入少量稀硫酸,目的是_____________。
6H2O溶液时,需加入少量稀硫酸,目的是_____________。
(2)得到的草酸亚铁沉淀需充分洗涤,检验是否洗涤干净的方法是_____________。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
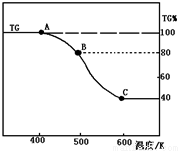
①则A-B发生反应的化学方程式为_____________;
②已知B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式_____________;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g样品,溶于少量2mol/L硫酸中并用100mL容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V1 mL。
Ⅲ.向上述溶液中加入足量Zn粉,使溶液中的Fe3+恰好全部还原为Fe2+,过滤。
Ⅳ.洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液。
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V2 mL。
回答下列问题:
①已知:草酸(H2C2O4)与酸性高锰酸钾溶液反应,现象是有气泡产生,紫色消失,写出该反应的离子方程式:_____________;
②若省略步骤Ⅳ,则测定的草酸根离子含量 (填“偏大”、“偏小”或“不变”)。
③m g样品中草酸根离子的物质的量为_____________(用c,V1,V2的式子表示,不必化简)
查看答案和解析>>
科目:高中化学 来源:2017届湖南衡阳八中高三实验班暑期第一次月考理综化学(解析版) 题型:选择题
下列各组离子一定能大量共存的是
A.某无色透明的酸性溶液:Cl-、Na+、MnO4-、SO42-
B.能使pH试纸变深蓝色的溶液:Na+、NH4+、K+、CO32-
C.加入过量NaOH溶液后可得到澄清的溶液:K+、Ba2+、HCO3-、Cl-
D.常温下pH=12的溶液: K+、Ba2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高二下期末化学试卷(解析版) 题型:选择题
五种短周期主族元素A、B、C、D、E的原子序数依次递增,A2属于绿色燃料,C的氧化物常用于玻璃的生产,D元素原子的核电荷数是同主族上一周期元素的2倍,B、C为同周期元素,B、D原子最外层电子数之和等于E的最外层电子数. 根据以上叙述,下列说法中正确的是( )
A. 五种元素中B元素的金属性最强
B. 元素D、E分别与元素A形成化合物的稳定性:A2D>AE
C. 元素C、D、E的最高价氧化物对应水化物的酸性递减
D. 元素B、D、E的简单离子半径大小为:B>D>E
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高二下期末化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是( )
A.将铜插入稀硝酸中:Cu+4H++2NO3﹣═Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+3H+═H2SiO3↓+3Na+
查看答案和解析>>
科目:高中化学 来源:2017届河北沧州市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某水溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-中的若干种离子。某同学取100ml的溶液分成两等份进行如下实验:
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲。
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体。
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到 11.65g固体。
据此,该同学得到的结论正确的是
A.实验①中产生的气体为氨气,并可得原溶液中c(NH4+)=0.2 mol·L-1
B.实验③中的白色沉淀中一定有BaSO4,无BaCO3
C.原溶液中一定有K+,且c(K+)=0.4 mol·L-1
D.若要判断原溶液中是否有Cl-,无需另外设计实验验证
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下学期期末化学卷(解析版) 题型:填空题
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如如图所示:

(1)从反应开始到10 s时,用Z表示的反应速率为________,X的物质的量浓度减少了______,Y的转化率为________。
(2)该反应的化学方程式为_______________________________________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如如图所示。则下列说法符合该图像的是________。

A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com