
下列说法正确的是( )
A.需要加热的化学反应都是吸热反应
B.中和反应都是放热反应
C.原电池是将电能转化为化学能的一种装置
D.水力发电是将化学能转化为电能的过程
科目:高中化学 来源: 题型:
某烯烃与氢气加成后得到2,2-二甲基丁烷,该烯烃的名称是
A.2,2-二甲基-3-丁烯 B.2,2-二甲基-2-丁烯
C.2,2-二甲基-1-丁烯 D.3,3-二甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下 列实验测定:①准确称取1.7700 g样品,配制成100.00 mL溶液A。②准确量25.00mL 溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白 色固体0.5825 g。③准确量取25.00 mL溶液A,加适量稀硫酸酸化后,用0.020 0mol· L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液25.00 mL。H2O2与KMnO4反应的离子方程式 如下:2MnO4-+5H2O2+6H+===2Mn2++8H2O+5O2↑
(1)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-6mol·L-1,应保 持溶液中c(Ba2+)≥_______mol·L-1。
(2)上述滴定若不加稀硫酸酸化,MnO4-被还原为MnO2,其离子方程式为 。
(3)通过上述实验事实,该样品的组成为(写化学式) 。
(4)上述实验③KMnO4溶液滴定至终点的现象是)_____________¡£怎样判断滴定达到了 终点 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式如下图所示,它可发生的反应类型有:( )
 ①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚
①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚
A.①②③⑤⑥ B.②③④⑤⑧
C.①②③⑤⑥⑦ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
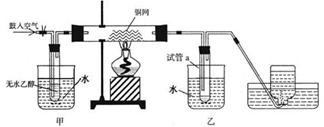 某小组用下列装置进行乙醇催化氧化的实验。⑴实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式 。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。⑵甲和乙两个水浴作用不相同。甲的作用是 ;乙的作用是 。
某小组用下列装置进行乙醇催化氧化的实验。⑴实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式 。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。⑵甲和乙两个水浴作用不相同。甲的作用是 ;乙的作用是 。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可在混合液中加入 (填写字母)。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)====CO2(g)+3H2(g);△H=+49.0kJ·mol-1
②CH3OH(g)+1/2O2(g)====CO2(g)+2H2(g); △H=-192.9kJ·mol-1

下列说法正确的是
A.CH3OH的燃烧热为192.9kJ·mol-1
B.反应①中的能量变化如上图所示
C.CH3OH转变成H2的 过程一定要吸收能量
过程一定要吸收能量
D.根据②推知反应CH3OH(1)+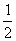 O2(g)====CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
O2(g)====CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+ O2(g)==CO(g);△H=-393.5 kJ/mol
O2(g)==CO(g);△H=-393.5 kJ/mol
B.2H2(g)+O2(g)==2H2O(g);△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)==CO2(g)+2H2O(g);△H=-890.3 kJ/mol
D. C6H12O6(s)+3O2(g) === 3CO2(g)+3H2O(1);△H=-1400 kJ/mol
C6H12O6(s)+3O2(g) === 3CO2(g)+3H2O(1);△H=-1400 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CO(g)+O2(g)====2CO2(g) ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)====Na2CO3(s)+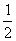 O2(g) ΔH=-226 kJ/mol
O2(g) ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
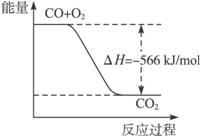
A.CO的燃烧热为283 kJ
B.上图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)====2Na2CO3(s)+O2(g) H>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________。
⑵ 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
⑶ 下列可用于测定TiO2粒子大小的方法是_____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
⑷ 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。




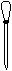

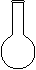

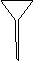

a b c d e
⑸ 滴定终点的现象是___________________________________________________。
⑹ 滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为________ _________________。
_________________。
⑺ 判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果_________________________。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com