
科目:高中化学 来源: 题型:
取化学式为MZ的黄色粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水。按图连接仪器。
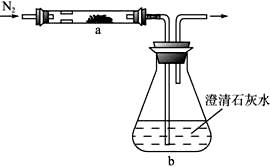
实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。根据以上叙述回答问题:
(1)元素Z是 :
(2)停止加热前是否需要先断开a和b的连接处?为什么?
;
(3)反应管a中发生的所有反应的化学方程式是
;
(4)本实验的尾气是否需处理?如需处理,请回答如何处理:如不需处理,请说明理由。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是 ( )
A.在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸
B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜加快反应速率
C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
取100mLNa2CO3和Na2SO4的混合液,加入过量BaCl2溶液后得到10.21g白色沉淀,用过量稀硝酸处理后沉淀质量减少到2.33g,并有气体放出。试计算:
①原混合物中Na2CO3和Na2SO4的物质的量浓度。
②产生的气体在标准状况下的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
I2在KI溶液中存在平衡:  ,某I2、、KI混合溶液中, c(
,某I2、、KI混合溶液中, c( )与温度T的平衡曲线图如下。下列说法不正确的是
)与温度T的平衡曲线图如下。下列说法不正确的是

A. 反应 的△H>0
的△H>0
B.若温度为 ,反应的平衡常数分别为
,反应的平衡常数分别为
C.若反应进行到状态D时,一定有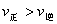
D.状态A与状态B相比,状态A的c(I2) 小
查看答案和解析>>
科目:高中化学 来源: 题型:
碘与氢气反应的热化学方程式是
①I2(g)+H2(g) 2HI(g)ΔH=-9.48 kJ·mol-1 ②I2(s)+H2(g)
2HI(g)ΔH=-9.48 kJ·mol-1 ②I2(s)+H2(g) 2HI(g)ΔH=+26.48 kJ·mol-1 下列说法正确的是( )
2HI(g)ΔH=+26.48 kJ·mol-1 下列说法正确的是( )
A. 从上述两反应可知1mol的I2(g)能量比1mol的I2(s)能量高
B. I2(s) I2(g) ΔH<0
I2(g) ΔH<0
C. ②的反应物总能量与①的反应物总能量相等
D. 1 mol I2(g)中通入1 mol H2(g),发生反应时放出的热量为9.48 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式,正确的是( )。
A.澄清石灰水中通入过量二氧化碳:Ca2++2OH- +CO2 ===CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅:CO32- +SiO2==SiO32- +CO2↑
C.二氧化硅与烧碱溶液反应:SiO2 +2OH- ===Na2 SiO3+H2O
D.硅酸与烧碱溶液中和:H2SiO3 +2OH- === SiO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
|
| 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) H= —456 kJ·mol-1
已知:
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
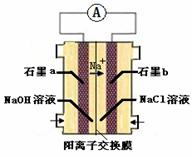
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com