
����Ŀ��������ͼװ�òⶨ�к��ȵ�ʵ�鲽�����£�
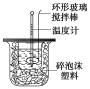
������Ͳ��ȡ50 mL 0.25 mol/L���ᵹ��С�ձ��У����������Һ�¶ȣ�
������һ��Ͳ��ȡ50 mL 0.55 mol/L NaOH��Һ����������¶ȣ�
�۽�NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ�������Һ����¶ȡ�
�ش��������⣺
(1)����NaOH��Һ����ȷ������_________
A���ز������������� B���������������� C��һ��Ѹ�ٵ���
(2)ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������__________
A�����¶ȼ�С�Ľ��� B���ҿ�ӲֽƬ�ò��������� C����������ձ� D���������¶ȼ��ϵĻ��β�������������س鶯
(3)ʵ���������±���
�¶� ʵ������� | ��ʼ�¶�t1�� | ��ֹ�¶�t2/�� | �¶Ȳ�ƽ��ֵ (t2��t1)/�� | ||
H2SO4 | NaOH | ƽ��ֵ | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
�ٸ��ݱ������ݼ�������¶Ȳ��ƽ��ֵΪ______����
�ڽ�����Ϊ0.55 mol/L NaOH��Һ��0.25 mol/L������Һ���ܶȶ���1 g/cm3���кͺ�������Һ�ı�����c��4.18 J/(g����)�����к�����H��_______( ȡС�����һλ)��
������ʵ����ֵ������к���Ϊ57.3 kJ/mol��ƫ�����ƫ���ԭ�������____��
a��ʵ��װ�ñ��¡�����Ч���� b�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶� c����ȡNaOH��Һ�����ʱ���Ӷ��� d���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
���𰸡�C D 3.4 -56.8kJ/mol abcd
��������
��ʵ���Ŀ���Dzⶨ�к��ȣ��к�����ָ��ǿ���ǿ���ϡ��Һ��ȫ��Ӧ����1molˮ�ų�����������ʵ�������Ȳⶨ��ͼӦǰ���¶ȣ�Ȼ��ⶨ��Ӧ��ֹ�¶ȣ�Ȼ�����ñ����ݽ��¶�ת��Ϊ����������к��ȡ���ʵ����Ϊ��֤��ͼ���ȫ��Ӧ��NaOH������ʵ��Ĺؼ���Ҫ���¡�
(1)Ϊ�˼���������ɢʧ��ʵ������е���NaOH��Һʱ������һ��Ѹ�ٵĵ��룬����ѡC��
(2)�¶ȼ��Dz����¶ȵģ�����ʹ���¶ȼƽ��裻Ҳ������������ձ���������ܵ���Һ�彦��������ɢʧ��Ӱ��ⶨ����������ܴ�ӲֽƬ�ò��������裬�����������ɢʧ��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ���������ǣ��������¶ȼ��ϵĻ��β������������ؽ���������ѡD��
(3)���Ĵε��²�ֱ�Ϊ3.4����5.1��3.3����3.5������2������ƫ��ϴ���ȥ������ƽ���²�Ϊ![]() =3.4����
=3.4����
��50mL0.25mol/L������50mL0.55mol/LNaOH��Һ�����кͷ�Ӧ��NaOH��������������ˮ�����ʵ���Ϊ0.05L��0.25mol/L��2=0.025mol����Һ������Ϊ100ml��1g/cm3=100g���¶ȱ仯��ֵ��T=3.4����������0.025molˮ�ų�������ΪQ=mc��T=100g��4.18J/(g��)��3.4��=1421.2J����1.4212kJ������ʵ���õ��к��ȡ�H=-![]() =-56.8kJ/mol��
=-56.8kJ/mol��
��ʵ�����ľ���ֵС���к��ȵľ���ֵ��
a��ʵ��װ�ñ��¡�����Ч�������ɢʧ�ϴ������к��ȵľ���ֵƫС����a���ϣ�
b�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶ȣ��¶ȼ���մ�е�NaOH�����ᷴӦ�ų�������ʹ�òⶨ�ij�ʼ�¶�ƫ�ߣ������������ɢʧ���ⶨ���²�ƫС���к��ȵľ���ֵƫС����b���ϡ�
c����ȡNaOH��Һ�����ʱ���Ӷ������ᵼ�������������ƫ�������������������ɵ�ˮ�����ʵ������䣬�ų������������䣬�������NaOH��Һ���ƫ��ʹ���Һ������ƫ�����õ��²��ƫС���к��ȵľ���ֵƫС����c���ϣ�
d���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ��У�����ɢʧ�ϴ������к��ȵľ���ֵƫС����d���ϣ�
�ʴ�Ϊ��abcd��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������͡��һ��������������ɭ����ҩ���ϳ�·������ͼ���£�

(1) ��CH3CH2CH2NH2�����������ŵ����Ʒֱ�Ϊ ______�� ________��
��CH3CH2CH2NH2�����������ŵ����Ʒֱ�Ϊ ______�� ________��
(2)D��E�ķ�Ӧ������_______��
(3)B�ķ���ʽΪC12H12O2��д��B�Ľṹ��ʽ��____ ��
(4)C��һ��ͬ���칹��Xͬʱ��������������д��X�Ľṹ��ʽ��_______��
�ٺ��б�������ʹ��ˮ��ɫ��
���������������·���ˮ�⣬ˮ��������������̼ԭ����֮��Ϊ6��5������һ��ˮ���������к���3�ֲ�ͬ��ѧ��������ԭ�ӡ�
(5)��֪��![]()
![]() R3COOH+
R3COOH+![]() �����
�����![]() ��
��![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ� �ĺϳ�·������ͼ_______(���Լ����л��ܼ����ã��ϳ�·������ͼʾ�����������)��
�ĺϳ�·������ͼ_______(���Լ����л��ܼ����ã��ϳ�·������ͼʾ�����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ�У���ȷ���ǣ� ��
A.����ȼ����Ϊ890.3 kJmol-1���Ȼ�ѧ����ʽΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H=+890.3 kJmol��1
B.ϡ�����ϡ����������Һ��ϣ����Ȼ�ѧ����ʽΪ��H++OH-=H2O ��H=-57.3 kJmol��1
C.H2ȼ����Ϊ285.8kJmol��1��ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g)+O2(g)=2H2O(1) ��H=-571.6 kJmol��1
D.500�桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-38.6 kJ��mol-1
2NH3(g) ��H=-38.6 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѪҺ�д���![]() ��
��![]() �Ȼ���ԡ������£�ˮ��Һ�и�����Ե���Ũ��֮�ȵĶ���ֵIgx[x��ʾ
�Ȼ���ԡ������£�ˮ��Һ�и�����Ե���Ũ��֮�ȵĶ���ֵIgx[x��ʾ![]() ��
��![]() ��pH�Ĺ�ϵ��ͼ��ʾ����֪̼��pKa1��6.4������pKa2��7.2(pKa����lgKa)��������˵����ȷ����
��pH�Ĺ�ϵ��ͼ��ʾ����֪̼��pKa1��6.4������pKa2��7.2(pKa����lgKa)��������˵����ȷ����

A.����I��ʾlg![]() ��pH�ı仯��ϵ
��pH�ı仯��ϵ
B.a��b�Ĺ����У�ˮ�ĵ���̶���С
C.��pH����ʱ��![]() ��С
��С
D.��c(H2CO3)��c(HCO3��)ʱ��c(HPO42��)��c(H2PO4��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�ѡ����,����֮��ͨ��һ����Ӧ����ʵ����ͼ��ʾ�仯���ǣ� ��
ѡ�� | �� | �� | �� | �� |
A | Al | AlCl3 | Al2O3 | NaAlO2 |
B | S | H2S | SO2 | SO3 |
C | Na | Na2O | NaOH | Na2O2 |
D | N2 | NH3 | NO | NO2 |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B����ѧ���������ʣ����������ӿɴӱ���ѡ��.
������ | K+��Na+��NH4+��Fe2+��Ba2+��Cu2+ |
������ | OH����I����NO3����AlO2����HCO3����HSO4�� |
��1����A��ˮ��ҺΪ��ɫ��B��ˮ��Һ�ʼ��ԣ�A��B��ˮ��Һ��Ϻ�ֻ����������ϡ����İ�ɫ��������ʹʪ��ĺ�ɫʯ����ֽ���������壬��:
��A�еĻ�ѧ������Ϊ_________���������Ӽ����������ۼ�������
��A��B��Һ��Ϻ���ȳ����ԣ��÷�Ӧ�����ӷ���__________________________ ��
��2����A��ˮ��ҺΪdz��ɫ��B����ɫ��Ӧ�ʻ�ɫ����A��ˮ��Һ�м���ϡ���������������ټ���B����Һ��ƣ���A��B��ˮ��Һ��Ϻ������Ա仯����
��A�Ļ�ѧʽΪ__________________________ ��
�ھ�����������������Һ��Ƶ�ԭ����������֣���������������
��._______________________����._________________________��
������һ������֤��������Һ��Ƶ�ԭ��_________________________��
������������������Һ���ԭ����������Ƴ�ԭ��أ���������a����b����b���ĵ缫��ӦʽΪ_��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��ԭ���������μ�С�����ֶ�����Ԫ�أ�C�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ��Aԭ����2��δ�ɶԵ��ӣ�A��C��D����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����壮E�ǵ�������Ԫ�أ���ԭ�Ӻ���������������Dԭ����ͬ�����������Ӿ�������
��ش��������⣨��Ԫ�ط��Ż�ѧʽ��ʾ����
��1��Ԫ��B��C��A�Ļ�̬ԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ__________________��
��2��M������Cԭ�ӹ�����ӻ�����Ϊ__________________��
��3��E+�ĺ�������Ų�ʽΪ__________________1s22s22p63s23p63d10
����ͼ����D��E�γɵ�ij�ֻ�����ľ����ṹʾ��ͼ���û�����Ļ�ѧʽΪ__________________��
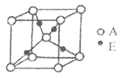
��4��������BD3�ķе�Ȼ�����CA4�ĸߣ�����Ҫԭ����__________________��
��5��д����CA2��Ϊ�ȵ������B3-�Ľṹʽ __________________��
��6����CrCl3��6H2O�ܽ�������ˮ�еõ�����ɫ��Һ����Һ��Cr3+��[Cr��H2O��5Cl]2+��ʽ���ڡ�������Һ�У������ڵ�������������__________________�����ţ���
A�����Ӽ� B�����ۼ� C�������� D����λ�� E�����»���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �ⶨ�����NaOH��Һ��Ӧ���к���ʱ��ÿ��ʵ���Ӧ���������¶ȣ����������ʼ�¶ȡ�NaOH��Һ����ʼ�¶Ⱥͷ�Ӧ�����ֹ�¶�
B. HCl��NaOH��Ӧ���к�����H=57.3 kJ��mol1����ϡH2SO4��ϡCa(OH)2��Һ��Ӧ���к��� ��H=2��57.3 kJ��mol1
C. ȼ������ָ��101 kPaʱ��ȼ����ȫȼ��ʱ���ų�������
D. S(s)+ ![]() O2(g)
O2(g)![]() SO3(g) ��H=315 kJ��mol1(ȼ����)
SO3(g) ��H=315 kJ��mol1(ȼ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ĵ��ʼ��仯������;�dz��㷺���ش���������:
��1����̬��ԭ�Ӽ۵��ӹ����ʾʽΪ______________________���ĵ�һ�����ܱ��������ԭ����_____________________________________________��
��2����֪��Ӧ6P2H4==P4+ 8PH3����P2H4��������ԭ���ӻ�������________________��P4���ӵļ��ι�����________________________��
��3��N��Pͬ���塣
��NH3�ķе��PH3������ԭ����_________________________��NH3�����м��DZ�PH3�����м��Ǵ���ԭ����______________________________________________��
�ڵ�ԭ�Ӽ���γɵ���˫��������������ԭ��֮�������γ�˫������������ԭ�ӽṹ�Ƕȷ�����ԭ����___________________________________________��
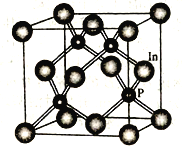
��4��������һ�ְ뵼����ϣ��侧������ͼ��ʾ����������Ϊa nm��In ����λ��Ϊ_______________����Inԭ�Ӽ����Ϊ![]() a nm ��In ԭ����________����
a nm ��In ԭ����________����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com