
| A��Cu��OH��2��CuCO3��CuS | B��Cu��OH��2��CuCO3��CuS |
| C��CuS ��Cu��OH��2��CuCO3 | D��CuS ��Cu��OH��2��CuCO3 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
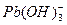 ��
��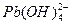 ,����̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ:
,����̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ: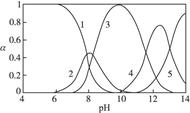
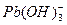 ,5��ʾ
,5��ʾ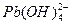
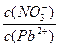 ___________2(�������=������);������Һ�е����Ȼ����Һ��,
___________2(�������=������);������Һ�е����Ȼ����Һ��, 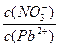 ����,���ܵ�ԭ����_____________��
����,���ܵ�ԭ����_____________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ˮ������Ҫ�ɷ���MgCO3��CaCO3 |
| B��Ӳˮ�������ǽ�ȫ����Mg2+��Ca2+���� |
| C������FeS��MnS�Գ�ȥ��ҵ��ˮ�е�Cu2����Cd2����Pb2�����ؽ������� |
| D��θ��ƽ����Ҫ�ɷ�������������������θ�������ͬʱҲ�ɲ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1.8��10��9 mol/L | B��1.9��10��10 mol/L |
| C��5.9��10��10 mol/L | D��5.9��10��9 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaOH | B��ʯ��ˮ | C��ͭƬ | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڢۢ� | B���٢ڢ� | C���ۢܢ� | D��ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��
| B��
| C��14+
| D��14+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ͬŨ�ȵ�Na2SO4��Na2CO3�����Һ�еμ�BaCl2��Һ��BaSO4������ | ||||||||
| B��BaCO3������Һ�м���������������ˮ��c��Ba2+������ | ||||||||
C��BaSO4��BaCO3���������Һ��
| ||||||||
| D��BaSO4����Һ�м���Na2CO3Ũ��Һ��BaSO4������ת��ΪBaCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����AgCl������������ | B����AgCl�������� |
| C���г���������������AgCl | D����ȷ���Ƿ��г������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com