
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属键是金属阳离子与自由电子间的相互作用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属具有光泽是因为金属阳离子吸收并放出可见光
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.鸡蛋壳浸泡在盐酸中产生气泡:CO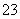 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
B.四氧化三铁固体溶解在稀硝酸中: Fe3O4+8H+===2Fe3++Fe2++4H2O
C.将氨气通入硫酸溶液中: NH3+H+===NH
D.向碳酸氢铵溶液中加入足量的NaOH溶液: NH +OH-===NH3·H2O
+OH-===NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生做乙醛还原性的实验,取1 mol·L-1的硫酸铜溶液2 mL和0.4 mol·L-1的氢氧化钠溶液4 mL,在一个试管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无砖红色沉淀,实验失败的原因是( )
A.氢氧化钠的量不够 B.硫酸铜的量不够
C.乙醛溶液太少 D.加热时间不够
查看答案和解析>>
科目:高中化学 来源: 题型:
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体。下列关于物质X的说法正确的是( )
A.X分子式C6H8O7
B.1 mol物质X可以和3 mol氢气发生加成
C.X分子内所有原子均在同一平面内
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
解析:(1)利用“N”守恒可知需m(NaN3)= ×
×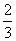 ×65 g·mol-1=78 g。
×65 g·mol-1=78 g。
(2)①由反应方程式可知产生1 mol H2同时生产2 mol OH-,故c(OH-)=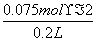 =0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
=0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
(3)若溶液仅含NaAl(OH)4,利用方程式可知得到24 mol Al(OH)3的同时生成12 mol Na2CO3,而实际得到24 mol Al(OH)3 与15 mol Na2CO3,说明溶液中含有NaOH,且NaOH优先与CO2反应生成Na2CO3,利用Na守恒知溶液中n(NaOH)=(15-12) mol×2=6 mol,故通入 112 L (5 mol)CO2先与NaOH作用消耗3 mol CO2生成3 mol Na2CO3,然后2 mol CO2与NaAl(OH)4作用得到4 mol Al(OH)3和2 mol Na2CO3,故n[Al(OH)3]∶n(Na2CO3)=4∶(3+2)=4∶5。
(4)由NaOH+HCl===NaCl+H2O可知溶液pH=7时,二者恰好反应完全,故三次实验得到的固体均为纯净氯化钠,利用“钠守恒”得 =
=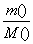 ,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。
,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。
答案:(1)78 (2)①c(OH-)=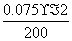 ×1 000=0.75 (mol/L)
×1 000=0.75 (mol/L)
②设上述合金中含a mol钠、b mol钾,则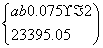
a=0.050 b=0.10
该钠—钾合金的化学式为NaK2。
(3)溶液含氢氧化钠。氢氧化钠和二氧化碳反应生成碳酸钠:15-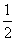 ×24=3 (mol)
×24=3 (mol)
112 L二氧化碳的物质的量: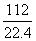 =5 (mol)
=5 (mol)
n[Al(OH)3]∶(Na2CO3)=[(5-3)×2]∶5=4∶5
(4)由氯化钠的质量推算,氢氧化钠样品的摩尔质量为
M1(氢氧化钠)= ×2.40=40 (g/mol)
×2.40=40 (g/mol)
M2(氢氧化钠)=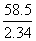 ×2.32=58 (g/mol)
×2.32=58 (g/mol)
M3(氢氧化钠)= ×3.48=58 (g/mol)
×3.48=58 (g/mol)
结论:
实验①所取氢氧化钠样品是NaOH;
实验②和实验③所取氢氧化钠样品应该是NaOH·H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生对SO2与漂粉精的反应进行实验探究:
| 操作 | 现象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
|
| i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是 ________________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是______________________。
(3)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成。进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
① 实验a的目的是_____________________________________________________。
②由实验a、b不能判断白雾中含有HCl,理由是________________________________。
(4)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是______________________
________________________。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
②用离子方程式解释现象iii中黄绿色褪去的原因:__________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气和水。反应中生成的氧化产物和还原产物的物质的量之比是( )
A.1:3 B.2:3 C.1:1 D. 4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、油脂、蛋白质是维持人体生命活动所必需的三大营养物质。下列说法你认为正确的是( )
①淀粉是人体所需能量的主要来源
②油脂在酸性条件下水解生成甘油和肥皂
③蛋白质水解生成氨基酸
④用平行光照射蛋白质溶液,在垂直光线的方向可看到一条明亮的通路
⑤植物油是高级脂肪酸甘油酯,属于高分子化合物
⑥淀粉、纤维素均属于多糖,二者的分子式均为(C6H10O5)n,互为同分异构体
A.②③④ B.①③⑤
C.①③④ D.②⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com