
【题目】普伐他汀是一种调节血脂的药物,其结构如右图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是
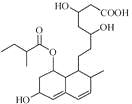
A. 能与FeCl3溶液发生显色反应
B. 能使酸性KMnO4溶液褪色
C. 1mol该物质与足量钠发生反应生成4molH2
D. 1mol该物质最多可与1molNaOH反应
科目:高中化学 来源: 题型:
【题目】有机物A是一种重要的化工原料,以A为主要起始原料,通过下列途径可以合成高分子材
料PA及PC。

试回答下列问题
(1)B的化学名称为________,B到C的反应条件是_____________。
(2)E到F的反应类型为__________,高分子材料PA的结构简式为________。
(3)由A生成H的化学方程式为______________________。
(4)实验室检验有机物A,可选择下列试剂中的_____________。
a.盐酸 b.FeCl3溶液 C. NaHCO3溶液 d.浓溴水
(5)E的同分异构中,既能与碳酸氢钠溶液反应、又能发生银镜反应的有机物共有_____种。其中核磁共振氢谐图有5组峰,且峰面积之比为6:1:1:1:1的物质的结构简式为____。
(6)由B通过三步反应制备1.3-环己二烯的合成路线为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用甲酸钠(HCOONa)制备Na2S2O4并测定产品的纯度,实验装置(夹持、加热仪器略)如图

将反应液分离提纯得到Na2S2O4产品,取产品mg溶于水,并定容为100mL,取25.00mL加入锥形瓶中,加入NaOH溶液及指示剂,用cmol·mol-1的K3[Fe(CN)6]标准溶液进行滴定{4K3[Fe(CN)6]+2Na2S2O4+8NaOH=3K4[Fe(CN)6]+4Na2SO3+Na4[Fe(CN)6]+4H2O},滴定至终点时,消耗标准液VmL。则产品的纯度为________(写出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乳酸薄荷醇酯(![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D. CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 恒温恒压下,在容积可变的器皿中,反应2NO2 (g)![]() N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.减小 B.增大 C.不变 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )

A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某有机物A的结构简式如右图,请按要求写出相应产物的结构简式
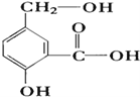
①A跟NaOH溶液反应 ____________________________;
②A跟NaHCO3溶液反应 _________________________________;
③A跟Na反应 _______________________。
(2)丙酸丙酯是一种香料,可以用下面的方案合成:![]()
①写出A,B,C,D的结构简式:
A ____________B_____________C_____________D_______________
②D有很多同分异构体,其中含有羧基的同分异构体中,烃基上的一氯代物有2种的结构简式为________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOH、H2SO3是中学化学中常见的弱酸,请回答下列问题:
(1)常温下,下列叙述能证明CH3COOH为弱酸是_________。
a. CH3COONa 溶液的pH大于7;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,PH > 2
(2)常温下,向0.1 mol·L-1 CH3COOH溶液中加蒸馏水稀释,稀释后,下列各量增大的是_________:
a.![]() b.
b.![]() c.c(OH-)
c.c(OH-)
(3)将浓度均为0.1mol/LCH3COOH和CH3COONa溶液等体积混合,测得混合液中c(CH3COO-)>c(Na+),则下列关系式中正确的是(_____)
A.c(H+) > c(OH-) B.c(H+) < c(OH-)
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COOH) + c(CH3COO-)=0.1mol/L
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液呈_______(填“酸性”,“中性”或“碱性”),原因是 _______________(用离子方程式表示)。若将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+) ___________c(CH3COO-) (填“ >” 或“=”或“<” )。
(5)25℃时,H2SO3的电离常数Ka1=1×10-2mol/L,Ka2=6×10-3mol/L,则该温度下NaHSO3的水解平衡常数Kh=__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H(3-溴-5-甲氧基苯甲酸甲酯)是重要的有机物中间体,可以由A(C7H8)通过下图路线合成。

请回答下列问题:
(1)C的化学名称为________,G中所含的官能团有醚键、_______(填名称)。
(2)B的结构简式为________,B生成C的反应类型为___________。
(3)由G生成H的化学方程式为___________。
(4)化合物F的同分异构体中能同时满足下列条件的共有________种。
①氨基和羟基直接连在苯环上 ②苯环上有三个取代基且能发生水解反应
(5)设计用对硝基乙苯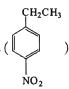 为起始原料制备化合物
为起始原料制备化合物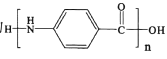 的合成路线(其他试剂任选)。_________________________
的合成路线(其他试剂任选)。_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com