
某合作学习小组讨论辨析下列说法,其中正确说法的数目为
①碱性氧化物都是金属氧化物,酸酐都是氧化物
②AlCl3溶液和Al(OH)3胶体的本质区别在于是否有丁达尔效应
③若规定0.024kg12C含有的原子数为阿伏加德罗常数,则标准状况下44gCO2的体积约为44.8L
④标准状况下,气体体积的大小取决于粒子数目和粒子间的平均距离
⑤同温同压下,等质量的二氧化硫气体和二氧化碳气体密度比为16:11,体积比为11:16
⑥把0.05mol氢氧化钡固体加入到100ml 1.0vmol/L盐酸中,溶液导电性基本不变
⑦活泼金属钾、钙、钠、镁、铝均由电解对应的熔融氧化物制得
⑧合金熔点、硬度都低于成分金属,青铜是使用最早的合金,钢是用量最大用途最广的合金
⑨同素异形体:C60、12C、金刚石、石墨
⑩工业合成氨是人工固氮的主要方法,工业生产玻璃、水泥、 冶炼铁都需要用到的原料是石灰石
冶炼铁都需要用到的原料是石灰石
A.3 B.5 C.4 D .7
科目:高中化学 来源: 题型:选择题
| A. | 过氧乙酸具有强氧化性,可以杀菌消毒,所以常用作消毒剂 | |
| B. | 黄瓜含有丰富的维生素C,热锅爆炒能减少维生素C的流失 | |
| C. | 向尿液中加入新制的Cu(OH)2悬浊液并加热煮沸可用于糖尿病诊断 | |
| D. | 可用燃烧的方法鉴别羊毛围巾和合成纤维围巾 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:实验题
Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。

已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
II.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_____________。
(2)吸收塔中的原料B可以选用____________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。
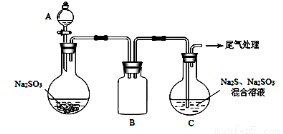
①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是______________。装置B的作用是___________________。
②C中制备Na2S2O3发生的连续反应有:Na2S +H2O +SO2=Na2SO3 +H2S、____________和__________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
有五组同族元素的物质,在101.3kPa时测定它们的沸点( )如下表所示:
)如下表所示:
① | He-268.8 | (a)-249.5 | Ar-185.8 | Kr151.7 |
② | F2-187.0 | Cl2-33.6 | (b)58.7 | I2184.0 |
③ | (c)19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
④ | H2O100.0 | H2S-60.0 | (d)-42.0 | H2Te-1.8 |
⑤ | CH4-161.0 | SiH4-112.0 | GeH4-90.0 | (e)-52.0 |
对应表中内容,下列各项中正确的是
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第④组中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te
C.第②组物质均有氧化性;第③组物质对应水溶液均是强酸
D.上表中同族物质对应的氢化物的沸点,均随相对分子质量的增大而升高
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
将amol硫化亚铁放入含3a mol H2SO4的浓硫酸中,充分反应后,氧化、还原产物分别是Fe3+、S和SO2,则:①硫化亚铁全部溶解 ②放出的气体少于1.5a mol③反应过程中转移5a mol e- ④放出1.5a mol气体 ⑤无法确定。上述叙述正确的是
A.①② B.②③ C.①④ D.⑤
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
. HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).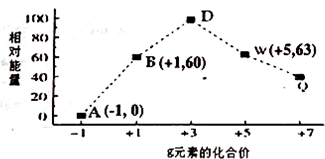
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
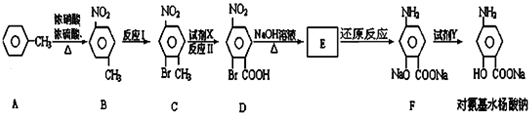
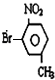 或
或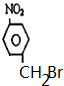 .
.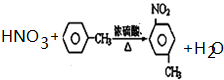 (注明反应条件).
(注明反应条件).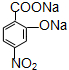 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
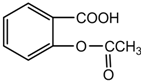 如图乙酰水杨酸又名阿斯匹林(Aspirin)具有退热、镇痛作用,常用于治疗伤风、感冒、头痛、神经痛及风湿性关节痛,近年来又用于防治老年性心血管病,但患有消化道溃疡的人不宜服用.对此化合 物不正确的说法是( )
如图乙酰水杨酸又名阿斯匹林(Aspirin)具有退热、镇痛作用,常用于治疗伤风、感冒、头痛、神经痛及风湿性关节痛,近年来又用于防治老年性心血管病,但患有消化道溃疡的人不宜服用.对此化合 物不正确的说法是( )| A. | 阿斯匹林的化学式为C9H8O4 | |
| B. | 该化合物具有酸性,能与 NaOH 或 NaHCO3反应 | |
| C. | 1 mol 该化合物与足量的 NaOH溶液反应,消耗 NaOH最大的物质的量为2 mol | |
| D. | 纯净的 Aspirin 不能与 FeCl3溶液反应,但它的水解产物能使FeCl3溶液显色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com