
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较Cl、Br的非金属性强弱 |
| B | 分别向MgCl2、AlCl3溶液中通入氨气 | 比较Mg、Al的非金属性强弱 |
| C | 将饱和碳酸钠溶液滴入稀硫酸中 | 比较S、C的非金属性强弱 |
| D | Fe、Cu分别与盐酸发应 | 比较Fe、Cu的非金属性强弱 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、在化学反应中某元素由化合态变为游离态,该元素一定被还原了 |
| B、失电子难的原子其得电子的能力一定强 |
| C、电子层结构相同的各种离子,它们的半径随核电荷数的增加而减小 |
| D、最外层电子数较少的金属元素,一定比最外层电子数较它多的金属元素活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯化钠的电子式为 | ||
B、镁的原子结构示意图为 | ||
C、氯化氢分子的形成过程可用电子式表示式: | ||
D、重水的化学式为
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) |
| B、b极上发生的电极反应是:4H2O+4e-═2H2↑+4OH- |
| C、c极上发生的电极反应是:O2+4H++4e-═2H2O |
| D、d极上进行还原反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:
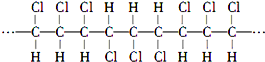 ;下列说法正确的是( )
;下列说法正确的是( )A、聚合物的链节是 |
| B、合成该聚合物的单体是CHCl═CHCl |
| C、聚合物的分子式是C3H3Cl3 |
| D、若n表示聚合度,则其相对分子质量为145.5n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位时间内生成n mol M,同时生成3n mol N |
| B、容器内混合气体的密度不随时间而改变 |
| C、W的生成速率与W的分解速率相等 |
| D、M、N、W的分子数之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
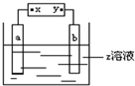 如图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板有无色无臭气体放出,符合a极板b极板x电极z溶液的是( )
如图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板有无色无臭气体放出,符合a极板b极板x电极z溶液的是( )| A、锌 石墨 负极 CuSO4 |
| B、石墨 石墨 负极 NaOH |
| C、银 铁 正极 AgNO3 |
| D、铜 石墨 负极 CuCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的d区,且原子序数是d区中最大的.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的d区,且原子序数是d区中最大的.| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com