
【题目】下列说法正确的是
A.1mol任何气体的体积都是22.4L
B.1molH2 的质量是1g,它所占的体积是22.4L
C.在标准状况下,1mol任何物质所占的体积都约为22.4L
D.在标准状况下,1mol任何气体所占的体积都约为22.4L
科目:高中化学 来源: 题型:
【题目】下列两组热化学方程式中,有关ΔH的比较正确的是( )
①CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH2
②NaOH(aq)+![]() H2SO4(浓)=
H2SO4(浓)=![]() Na2SO4(aq)+H2O(l) ΔH3
Na2SO4(aq)+H2O(l) ΔH3
NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH4
A.ΔH1>ΔH2;ΔH3>ΔH4 B.ΔH1>ΔH2;ΔH3<ΔH4
C.ΔH1=ΔH2;ΔH3<ΔH4 D.ΔH1<ΔH2;ΔH3<ΔH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种回收并利用含碘(I-)废液的工艺流程如下:
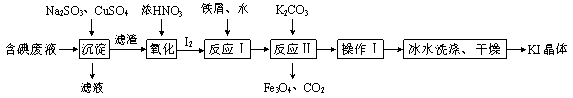
(1)“沉淀”中生成CuI的离子方程式为 。
(2)CuSO4的投加量对废水中I-的去除量影响较大,不同投加量(用过量系数表示)下,反应后I-和Cu2+的浓度如图所示,则适宜的CuSO4过量系数应为 ,分析原因___________。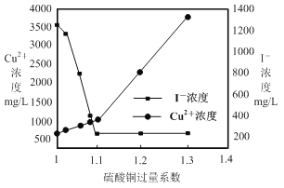
(3)反应Ⅰ中生成铁与碘的化合物(其中铁与碘的质量比为21:127),反应Ⅱ的化学方程式是_________。
(4)操作Ⅰ包括 ,冰水洗涤的目的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,不能达到实验目的的是

A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢和水蒸气
C.用装置丙可证明Cl2的氧化性强于S
D.用装置丁可以完成“喷泉”实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和联氨(N2H4)既是一种工业原料,又是一种重要的工业产品。
(1) 等物质的量的氨和联氨分别与足量二氧化氮反应,产物为氮气和水。则转移的电子数之比为___________。
(2) 联氨在一定条件下可按下式分解:3N2H4(g)=N2(g)+4NH3(g),已知断裂N-H、N-N及N≡N各1 mol需吸收的能量依次为390.8 kJ、193 kJ、946 kJ。若生成1 mol N2,则反应________(填“放出”或“吸收”)___ _______kJ的能量。
(3)NH3-O2燃料电池的结构如图所示。
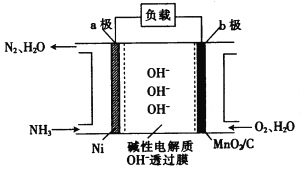
① a极为电池的________(填“正”或“负”)极。
②当生成1 mol N2时,电路中流过电子的物质的量为_____________。
(4)联氨可以高效地脱除烟道气中的NO从而生成 N2,该反应中氧化产物与还原产物的物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶澄清的溶液,其中可能含有NH![]() 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO![]() 、CO
、CO![]() 、SO
、SO![]() 、AlO
、AlO![]() 。取该溶液进行以下实验:
。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:A溶液从酸性变为碱性;B溶液逐渐产生沉淀;C沉淀完全溶解;D最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除________________的存在。
(2)由②可以证明________的存在;同时排除__________的存在;理由是_________ ______。
(3)由③可以证明________的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
c________________;d________________。
(4)由④可以证明____________的存在,同时排除____________的存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为______________,A电极的电极反应式为 ;反应进行一段时间后溶液C的pH将 (填“升高”“降低”或“基本不变”)。
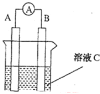
(2)我国首创以铝空气海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是________,负极反应为___________;正极反应为_______________________。
(3)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO32-4e-=4CO2,正极反应式为________________________,电池总反应式为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com