
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C (s)+2NO(g)CO2(g)+N2(g),平衡时c (NO)与温度T的关系如图所示,则下列说法正确的是( ) 
A.该反应的△H>0
B.若该反应在T1 , T2时的平衡常数分别为K1 , K2 , 则K1<K2
C.在T2时,若反应体系处于状态D,则此时v正>v逆
D.若状态B,C,D的压强分别为PB , PC , PD , 则 PC=PD>PB
【答案】C
【解析】解:A、由图可知,温度越高平衡时c(NO)越大,即升高温度平衡逆移,所以正反应为放热反应,即△H<0,故A错误;
B、该反应正反应是放热反应,升高温度平衡向逆反应移动,所以升温化学平衡常数减小,故K1>K2 , 故B错误;
C、T2时反应进行到状态D,c(NO)高于平衡浓度,故反应向正反应进行,则一定有υ(正)>υ(逆),故C正确;
D、达到平衡状态时,压强和温度成正比例关系,则PB=PD<PC , 故D错误.
故选C.
【考点精析】掌握化学平衡状态本质及特征是解答本题的根本,需要知道化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中进行下列反应:C(s)+CO2(g)═2CO(g);△H=+Q kJmol﹣1 . 如图为CO2、CO的物质的量随时间t的变化关系图.下列说法不正确的是( ) 
A.在0﹣1min内CO的物质的量增加了2mol
B.当固焦炭的质量不发生变化时,说明反应已达平衡状态
C.5min时再充入一定量的CO,n(CO)、n(CO2)的变化可分别由c、b曲线表示
D.3min时温度由T1升高到T2 , 重新平衡时K(T2)小于K(T1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示法不正确的是( )
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石) ΔH = +1.9 kJ·mol—1可知石墨比金刚石稳定
C.在稀溶液中:H++OH- ![]() H2O ΔH =-57.3 kJ·mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
H2O ΔH =-57.3 kJ·mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ
D.在热化学方程式中无论是反应物还是生成物必须表明聚集状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1 HA溶液中逐滴加入0.02 molL﹣1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,不正确的是( ) 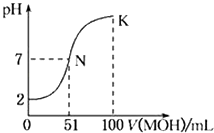
A.HA为一元强酸
B.MOH为一元弱碱
C.N点水的电离程度小于K点水的电离程度
D.K点对应的pH=10,则有c(MOH)+c(OH﹣)﹣c(H+)=0.005molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量: 。
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量: 。
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量: 。
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作中正确的是
A. 稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中,并不断搅拌
B. 过滤时,漏斗里液体的液面要高于滤纸的边缘
C. 胶头滴管的管口直接伸入试管里滴加液体,以免外溅
D. 实验结束后,用嘴吹灭酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是( )
A.Na、Mg、Al原子的失电子能力逐渐减弱
B.Si、P、S元素的最高正化合价依次降低
C.C、N、O的原子半径依次减小
D.Cl、Br、I的气态氢化物的稳态性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2 , 且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是( ) 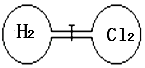
A.开始时左右两室分子数相同
B.最终容器内无H2存在
C.反应前后H2室压强相同
D.最终容器内密度与原来相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com