
【题目】下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色。化台物H和I两种气体相遇时产生白烟。化合物G的焰色反应为黄色。反应①和②均在溶液中进行。
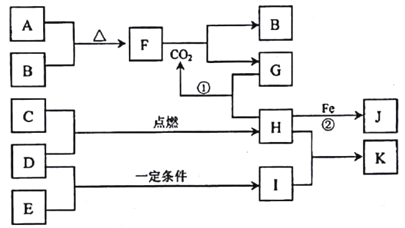
请按要求回答下列问题。
(l)写出下列物质的化学式:D________、F_______________。
(2)反应①的离子方程式为_____________。
(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为__________。
(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色,该反应的离子方程式为_________。这说明单质C的氧化性_______于单质碘(填“强”或“弱”)。
(5)向J溶液中滴入NaOH溶液时,生成的灰白色沉淀迅速变成灰绿色,最后变成红褐色。写出沉淀由灰白色变成红褐色的化学方程式:______________。
【答案】 H2 Na2O2 2H++CO32-=H2O+CO2↑ 产生白色沉淀 Cl2+2I-=I2+2Cl- 强 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】A、B、C、D、E都是短周期元素的单质,C为黄绿色气体,则C为Cl2,化合物H和I两种气体相遇时产生白烟,则D为H2,H为HCl,E为N2,I为NH3,生成K为NH4Cl,反应②为Fe与盐酸反应,则J为FeCl2,化合物G的焰色反应为黄色,与盐酸反应生成CO2,则G为Na2CO3或NaHCO3,A是固体,其余都是气体,结合元素守恒及转化关系可知,A为Na,B为O2,A、B反应生成F,则F为Na2O2,由F与二氧化碳的反应确定G只能为Na2CO3,则
(1)由上述分析可知D为H2,F为Na2O2;(2)反应①为盐酸与碳酸钠的反应,该离子反应为2H++CO32-=H2O+CO2↑;(3)K为NH4Cl,加入硝酸酸化的硝酸银溶液有氯化银沉淀生成,实验现象是出现白色沉淀;(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色,是因氯气氧化碘离子生成碘单质,离子反应为Cl2+2I-=I2+2Cl-,则氯气的氧化性强于碘的氧化性;(5)J为FeCl2,滴入NaOH溶液时,生成的灰白色沉淀迅速变成灰绿色,最后变成红褐色,发生4Fe(OH)2+O2+2H2O=4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】如图所示水槽中试管内有一枚铁钉,放置数天后观察:
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于腐蚀。
(2)若试管内液面上升,则原溶液呈性,发生腐蚀,电极反应式为:负极: , 正极:。
(3)若试管内液面下降,则原溶液呈性,发生腐蚀。电极反应式为,负极: , 正极:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个一氧化氮(NO)分子的质量为ag,一个二氧化氮(NO2)分子的质量为bg,NA表示阿伏加德罗常数,则氧原子的摩尔质量为
A.(a-b)NA gmol-1B.(b-a)NA gmol-1
C.(a-b)NA gD.(b-a)NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列排列顺序不正确的是
A.原子半径:Si> Na>OB.热稳定性:HF> HCl> H2S
C.碱性:CsOH> KOH> NaOHD.失电子能力:K> Na> Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:P4(g)+6Cl2(g)═4PCl3(g)△H=a kJmol﹣1 , P4(g)+10Cl2(g)═4PCl5(g)△H=bkJmol﹣1 , P4具有正四面体结构,PCl5中P﹣Cl键的键能为c kJmol﹣1 , PCl3中P﹣Cl键的键能为1.2c kJmol﹣1 . 下列叙述正确的是( )
A.P﹣P键的键能大于P﹣Cl键的键能
B.可求Cl2(g)+PCl3(g)═PCl5(s)的反应热△H
C.Cl﹣Cl键的键能为 (b﹣a+5.6c)/4 kJmol﹣1
D.磷元素的非金属性比氯强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com