
短周期元素的离子M2+和N2―具有相同的电子层结构,则下列说法正确的是
| A.M2+的离子半径比N2―小 | B.M的原子序数比N小 |
| C.M和N原子的电子层数相等 | D.M和N原子最外层电子数相等 |
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、Q在元素周期表中的相对位置如下图:地壳中含量最大的三种元素已包含其中。关于这些元素的叙述不合理的是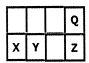
| A.最高价氧化物对应水化物的酸性Z>Y |
| B.原子半径X>Y |
| C.一定条件下,Q可分别与X、Y、Z形成化合物,这些化合物都可溶于NaOH溶液 |
| D.元素Y的氧化物是形成酸雨的罪魁祸首 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素, 它们的最高价氧化物的水化物之间相互反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,其低价氧化物具有漂白作用;W与Y可形成化合物W2Y。下列说法正确的是
| A.Y的低价氧化物与O3漂白的原理相同 |
| B.Y的氢化物和W2Y所含化学键的类型相同 |
| C.上述三种元素形成的简单离子,X离子半径最小 |
| D.工业上常用电解相应的盐溶液制备W、X的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y为短周期元素,X位于ⅠA族,X与Y可形成化合物X2Y,下列说法正确的是
| A.X的原子半径一定大于Y的原子半径 |
| B.X与Y的简单离子不可能具有相同的电子层结构 |
| C.两元素形成的化合物中,原子个数比不可能为1∶1 |
| D.X2Y可能是离子化合物,也可能是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是
| A.J和氢组成的化合物分子中只含有极性共价键 |
| B.工业上用电解熔融的M的氧化物方法来制备M |
| C.R、T两元素的气态氢化物中,T的气态氢化物更稳定 |
| D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各基态原子或离子的电子排布式错误的是
| A.Al 1s22s22p63s23p1 | B.S2- 1s22s22p63s23p4 |
| C.Na+ 1s22s22p6 | D.F 1s22s22p5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是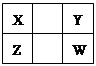
| A.Z元素的原子半径可能比Y元素的小 |
| B.Z的原子序数不可能是X的原子序数的2倍 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的最高价氧化物的水化物的酸性一定比W的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列结论错误的是
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
| A.只有① | B.①③ | C.②④⑤⑥⑦ | D.①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com