
在重水D2O中存在电离:D2O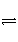
 D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
> 2 >
解析 本题综合了有关水的离子积、溶液的pH等知识,考查知识迁移与信息处理能力。解题关键是对pD定义和D2O离子积常数的理解。
由D2O的KW=1.6×10-15 mol2·L-2,得pKW=15-lg1.6,故纯D2O中,pD=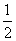 pKW=
pKW=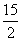 -
-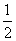 lg1.6>7。
lg1.6>7。
用0.01 mol DCl溶于D2O配成1 L溶液,在形成的DCl溶液中[D+]=0.01 mol·L-1
故pD=-lg[D+]=-lg 0.01=2。
用0.01 mol NaOD溶于D2O配成1L溶液,在形成的NaOD中,[OD-]=0.01 mol·L-1,pOD=2,pD=pKW-pOD=15-lg1.6-2=13-lg1.6>12。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
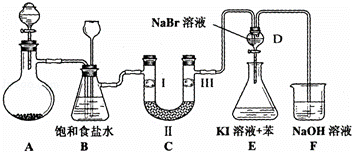
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为: .
(2)装置B中饱和食盐水的作用是 ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 .
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D.
A B C D
Ⅰ 干燥的有色布条 干燥的有色布条 湿润的有色布条 湿润的有色布条
Ⅱ 碱石灰 硅胶 浓硫酸 无水氯化钙
Ⅲ 湿润的有色布条 湿润的有色布条 干燥的有色布条 干燥的有色布条
(4)设计装置D、E的目的是 .打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是 .
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在密闭容器中充入SO3,发生化学反应:2SO32SO2+O2,反应一段时间后,又向其中充入18O2,在重新达到化学平衡状态后,18O原子存在于( )
A.SO3中 B.SO2中
C.O2中 D.三种物质中都有
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器内,800℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如表所示:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为________。
(2)下图中表示NO2变化曲线的是________,用O2表示从0~2 s内该反应的平均速率v=________。
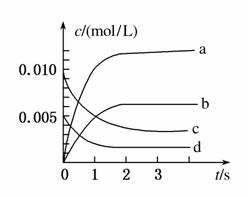
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃的下列溶液中,碱性最强的是( )
A.pH=11的溶液
B.[OH-]=0.12 mol·L-1
C.1 L中含有4 g NaOH的溶液
D.[H+]=1×10-10 mol·L-1的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
|
| A. | 常温常压下,1mol C2H4所含的电子数为12NA |
|
| B. | 标准状况下,16g甲烷中共价键数目为4NA |
|
| C. | 常温常压,4 g氦气所含的核外电子数为4NA |
|
| D. | 16g氧气和臭氧的混合物中含有1.5NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氢气在氯气中燃烧时产生苍白色火焰.在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,则下列关系式中一定正确的是( )
|
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有8 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为 ( )
A.8 g B.15.5 g C.11.7 g D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com