
| A. | 将氯气、铁按n(Cl2):n(Fe)=5:4混合点燃:5Cl2+4Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3+2FeCl2 | |
| B. | 将0.5molN2和1.5molH2于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 将大理石粉末置于FeCl3溶液中有气泡产生:2Fe3++3H2O+3CaCO3═2Fe(OH)3↓+3CO2↑+3Ca2+ | |
| D. | 将浓度均为0.1mol•L-1的NaOH、NH4HCO3等体积混合:NH4++OH-═NH3•H2O |
分析 A.与量无关,反应生成氯化铁;
B.合成氨的反应为可逆反应,热化学反应中为完全转化的能量变化;
C.反应生成氢氧化铁、氯化钙、二氧化碳;
D.等物质的量时,只发生氢氧根离子与碳酸氢根离子的反应.
解答 解:A.将氯气、铁按n(Cl2):n(Fe)=5:4混合点燃,发生3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故A错误;
B.将0.5molN2和1.5molH2于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)═2NH3(g)△H<-38.6kJ•mol-1,故B错误;
C.将大理石粉末置于FeCl3溶液中有气泡产生的离子反应为2Fe3++3H2O+3CaCO3═2Fe(OH)3↓+3CO2↑+3Ca2+,故C正确;
D.将浓度均为0.1mol•L-1的NaOH、NH4HCO3等体积混合的离子反应为HCO3-+OH-═CO32-+H2O,故D错误;
故选C.
点评 本题考查离子反应方程式及化学反应方程式的书写,为高频考点,把握物质的性质、发生的反应及离子反应的书写为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
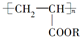 )的说法中,不正确的是( )
)的说法中,不正确的是( )| A. | 合成它的小分子化合物是CH3-CH2-COOR | |
| B. | 它可由CH2═CH-COOR经过加成聚合反应而得到 | |
| C. | 在一定条件下能发生水解反应 | |
| D. | 不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ③④⑤⑥ | C. | ②③⑤⑥ | D. | ①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ | |
| C. | 反应至4 min时,若HCl浓度为0.12 mol•L-1,则H2的反应速率为0.03 mol•(L•min-1) | |
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L-1的NaOH溶液中恰好反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 两种有机物的结构简式
两种有机物的结构简式 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca原子中的质子数和中子数都相等 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 几种核素具有相同的核电荷数,一定是同种原子 | |
| D. | 同种元素的不同核素之间互称同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com