
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如下图所示,试回答下列问题:
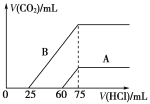
(1)原NaOH溶液的物质的量浓度为____________mol/L。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是____________,其物质的量之比为__________。
(3)曲线B表明,所得溶液加盐酸后产生CO2气体体积(标况)的最大值为 mL。
【答案】(1)0.75mol/L (2)NaOH、Na2CO3 3:1 (3)112mL
【解析】
试题分析:(1)加入75ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,
所以n(NaOH)=n(NaCl)=n(HCl)=0.075ml×0.1mol/L=0.0075mol,
所以c(NaOH)=![]() =0.75mol/L;
=0.75mol/L;
(2)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
当1/2<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当n(CO2):n(NaOH)≤1/2,反应按②进行,等于1/2,时,CO2、NaOH恰好反应生成Na2CO3;小于1/2时,生成Na2CO3,NaOH有剩余;
由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应,
反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(NaHCO3)=n(HCl)=(0.075-0.06)L×0.1mol/L=1.5×10-3mol,
根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×10-3mol,
由(1)可知,n(NaOH)=0.0075mol,
所以n(CO2):n(NaOH)=1.5×10-3mol:0.0075mol=1:5,小于1:2,所以反应按②进行,NaOH有剩余,溶液中溶质为Na2CO3和NaOH.
根据C原子守恒,所以n(Na2CO3)=n(CO2)=1.5×10-3mol,再根据钠离子守恒,
得溶液中氢氧化钠的物质的量为0.0075mol-1.5×10-3mol×2=0.0045mol,
所以溶液中NaOH与Na2CO3的物质的量之比为0.0045mol:1.5×10-3mol=3:1.
故答案为:Na2CO3、NaOH;1:3;
(3)由曲线B可知从25ml到75ml为碳酸氢钠与盐酸反应生成二氧化碳,
反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,
所以n(CO2)=n(HCl)=(0.075ml-0.025ml)×0.1mol/L=0.005mol,
所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL。


科目:高中化学 来源: 题型:
【题目】a,b,c,d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族,下列叙述正确的是
A.原子半径:d>c>b>a B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱 D.d单质的氧化性比a单质的氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. Na2O2吸收CO2产生O2 ,可用作呼吸面具供氧剂
B. ClO2具有还原性,可用于自来水的杀菌消毒
C. SiO2硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于300mL1mol·L-1盐酸与铁片的反应,其中能使反应速率加快的措施:
A. 升高温度
B. 再加300mL1mol·L-1盐酸
C. 用等量铁片代替铁粉
D. 改用100mL98%的硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53 kJ热量,则炭粉与氢气的物质的量之比为( )
A. 2∶3 B. 1∶2 C. 1∶1 D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源与我们日常生活密切相关,下列有关能源的叙述中不正确的是
A. 化石能源是不可再生的能源
B. 发展太阳能有助于减缓温室效应
C. 使用乙醇汽油可以减少汽车尾气排放造成的大气污染
D. 人类利用的能源都是通过化学反应获得的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中,能导电的是 ,属于电解质的是 (填序号)。
①氨气、②氨水、③NH3·H2O、④硫酸溶液、⑤干冰、⑥BaSO4、⑦金刚石
(2)将等物质的量的①Na、②Na2O、③Na2O2、④NaOH投入相同质量的水中,所得溶液浓度由大到小的顺序为 。如果将等物质的量换成等质量则 。(填序号)
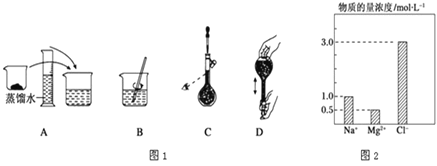
(3)如图表示某同学配制480mL 0.5mol/L 的NaOH溶液的部分操作示意图,其中有错误的是___________,这样操作所配制的溶液比要求的浓度要___________ (填“偏高”、“偏低”、“不影响”)。配制应称取___________gNaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2升的密闭容器中,发生以下反应:2A(g)+B(g)![]() 2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
A. 1.2 mol B. 1.6 mol C. 2.4 mol D. 2.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙醛(CH3CHO)和新制氢氧化铜的反应如下:
CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
某实验小组做上述反应时,发现NaOH的用量对反应产物有影响,于是他们采用控制变量的方法,均使用0.5 mL 40%的乙醛溶液进行下列实验。
编号 | 2%CuSO4溶液的体积 | 10%NaOH溶液的体积 | 振荡后 的现象 | pH | 加乙醛水浴加热后的沉淀颜色 |
1 | 2 mL | 3滴 | 浅蓝绿色沉淀 | 5~6 | 浅蓝绿色沉淀 |
2 | a | 15滴 | 浅蓝色沉淀 | 7~8 | 黑色沉淀 |
3 | 1 mL | 1 mL | 蓝色悬浊沉淀较少 | 9~10 | 红褐色沉淀 |
4 | b | 2 mL | 蓝色悬浊沉淀较多 | 11~12 | 红色沉淀 |
5 | 1 mL | 3 mL | 蓝紫色溶液 | 12~13 | ———— |
(1)上表中a、b应为 (填字母序号)。
A.15滴,1 mL B.2 mL,1 mL C.15滴,2 mL D.2 mL,2 mL
(2)查阅资料可知,实验1中的浅蓝绿色沉淀主要成份为Cu2(OH)2SO4,受热不易分解。写出生成Cu2(OH)2SO4反应的化学方程式 。基于实验1、2的现象可以得出结论:NaOH用量较少时, 。
(3)小组同学推测实验3中的红褐色沉淀可能是CuO和Cu2O的混合物,其理论依据是 。
(4)为了进一步证明实验4中红色沉淀的成分,该小组同学查阅资料得知:Cu2O在碱性条件下稳定,在酸性溶液中可转化为Cu2+、Cu。并进行了以下实验。
ⅰ.将实验4反应后的试管静置,用胶头滴管吸出上层清液。
ⅱ.向下层浊液中加入过量稀硫酸,充分振荡、加热,应观察到的现象是 。
(5)小组同学继续查阅资料得知:Cu(OH)2可与OH-继续反应生成蓝紫色溶液([Cu(OH)4] 2-),由此提出问题:[Cu(OH)4] 2-能否与乙醛发生反应,生成红色沉淀?设计实验解决这一问题,合理的实验步骤是 。基于上述实验,该小组同学获得结论:乙醛参与反应生成红色沉淀时,需控制体系的pH>10。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com