
����Ŀ����1�����᳧��β��ֱ���ŷŽ���Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ
��CH4��g����4NO2��g��===4NO��g����CO2��g����2H2O��g�� ��H����574 kJ��mol��1
��CH4��g����4NO��g��===2N2��g����CO2��g����2H2O��g�� ��H����1 160 kJ��mol��1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ___________________________��
��2����������������Դ��Ҳ����Ҫ�Ļ���ԭ�ϡ��������ɼ����Ʊ���CH4��g����H2O��l��===CO��g����3H2��g�� ��H����250.1 kJ��mol��1����֪298 Kʱ��CH4��g����CO��g����ȼ���ȷֱ�Ϊ890 kJ��mol��1��283 kJ��mol��1��д������ȼ���ȵ��Ȼ�ѧ����ʽ_______________________________��
��3������ͼ��ʾ��ʾ����NO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��____________________________________��

���𰸡�CH4(g)��2NO2(g)=CO2(g)��2H2O(g)��N2(g) ��H����867 kJ��mol��1 H2(g)��![]() O2(g)=H2O(l)����H����285.7 kJ��mol��1 NO2(g)��CO(g)=NO(g)��CO2(g)����H����234 kJ�� mol��1
O2(g)=H2O(l)����H����285.7 kJ��mol��1 NO2(g)��CO(g)=NO(g)��CO2(g)����H����234 kJ�� mol��1
��������
��1�����ݸ�˹������дNO2��ԭΪN2���Ȼ�ѧ����ʽ��
��2��������ȼ������1mol����ȼ������Һ̬ˮ�ų���������
��3������ͼʾ��NO2��CO��Ӧ����CO2��NO�ų�������368-134=234 kJ��
��1����CH4��g����4NO2��g��===4NO��g����CO2��g����2H2O��g�� ��H����574 kJ��mol��1 ��CH4��g����4NO��g��===2N2��g����CO2��g����2H2O��g�� ��H����1 160 kJ��mol��1�����ݸ�˹���ɢ�![]() +��
+��![]() ��CH4(g)��2NO2(g)=CO2(g)��2H2O(g)��N2(g) ��H����867 kJ��mol��1��
��CH4(g)��2NO2(g)=CO2(g)��2H2O(g)��N2(g) ��H����867 kJ��mol��1��
��2����CH4��g����H2O��l��===CO��g����3H2��g�� ��H����250.1 kJ��mol��1��
����298 Kʱ��CH4��g����CO��g����ȼ���ȷֱ�Ϊ890 kJ��mol��1��283 kJ��mol��1����֪
�� CH4��g����2O2��g��===CO2��g����2H2O��l����H����890 kJ��mol��1
��CO��g��+![]() O2��g��===CO2��g����H����283 kJ��mol��1��
O2��g��===CO2��g����H����283 kJ��mol��1��
���ݸ�˹���ɢ�![]() -��
-��![]() -��
-��![]() ������ȼ���ȵ��Ȼ�ѧ����ʽH2(g)��
������ȼ���ȵ��Ȼ�ѧ����ʽH2(g)��![]() O2(g)=H2O(l)����H����285.7 kJ��mol��1��
O2(g)=H2O(l)����H����285.7 kJ��mol��1��
��3������ͼʾ��NO2��CO��Ӧ����CO2��NO�ų�������368-134=234 kJ���Ȼ�ѧ����ʽ��NO2(g)��CO(g)=NO(g)��CO2(g)����H����234 kJ�� mol��1��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00 mL 0.1000 mol��L��1 NH3��H2O��Һ����εμ�0.1000 mol��L��1 HCl��Һ����ҺpH�����HCl��Һ����ı仯������ͼ��ʾ������˵����ȷ����

A. ����Һ��c(Cl��)>c(NH)>c(OH��)>c(H��)
B. ����Һ��c(NH)��c(Cl��)>c(OH��)��c(H��)
C. ����������������ʾ����Һ��ˮ�ĵ���̶Ȣ�>��>��
D. �ζ������в����ܳ��֣�c(NH3��H2O)>c(NH)>c(OH��)>c(Cl��)>c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ֪ʶ��գ�
(1)����ͨ�����ⷴӦ�ɵñ�ϩ����֪����C3H8(g) �� CH4(g)��C2H2(g)��H2(g) ��H1����156.6 kJ��mol��1��C3H6(g) �� CH4(g)��C2H2(g) ��H2����32.4 kJ��mol��1����ͬ�����£���ӦC3H8(g) �� C3H6(g)��H2(g)����H��______________ kJ��mol��1��
(2)Ϊ���ٴ�����Ⱦ��һЩ���й���������ʹ��CNG(ѹ����Ȼ��)���ȼ�ϣ�ʵ����0.16g������ȼ�ϣ���ȫȼ������224ml CO2(��״��)��0.36gҺ̬ˮ�����ų�8.903KJ����������д����CNG��ȫȼ�յ��Ȼ�ѧ����ʽ ____________________________________________________________
(3)��д��NH4Cl��Һ�и�����Ũ�ȵĴ�С��ϵʽ��______________________________________________
(4) ������ˮ��Һ�еĵ��뷽��ʽΪ___________________________________________
(5) ���з����У�����ʹ����ϡ��Һ��CH3COOH����̶��������_________(����ĸ���)��
A. �μ�����Ũ���� B������Һ C.��ˮϡ�� D���������������ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��һ����Ҫ�Ļ���ԭ�ϡ���֪A�ڱ�״���µ��ܶ�Ϊ1.16g��L-1��B�ɷ���������Ӧ������֮���ת����ϵ��ͼ����ش�

��1���л���A�к��еĹ�����������____________��
��2����Ӧ�ܵ�ԭ�������ʴ�100�����÷�Ӧ�Ļ�ѧ����ʽ��___________��
��3������˵����ȷ����___________��
A ��Ӧ�ݺϳ���������Ҳ��ʵ��ԭ��������100%
B.��Ӧ�ڡ��ۡ��ݵ���������ͬ
C ��������������ˮ��Ϊ��ɫҺ�壬���÷�Һ©������������������ˮ�Ļ����
D.��ͬ��������������������������Һ��ˮ�����ϡ�����и���ȫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��Ϊ�绯ѧװ�ã������й�������ȷ����(����)
A.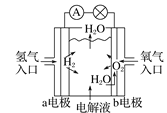 ����ȼ�ϵ��ʾ��ͼ�У�b�缫����������Ӧ
����ȼ�ϵ��ʾ��ͼ�У�b�缫����������Ӧ
B. ����Ȼ�ͭ��Һװ���У�������������ɫ����
����Ȼ�ͭ��Һװ���У�������������ɫ����
C. ���ʵ��װ���У������ǰ���缫������ȣ������ɺ����������Ϊ5.12 g������ʱ��������ƷӦ���Դ�������������·ת��0.08 mol����
���ʵ��װ���У������ǰ���缫������ȣ������ɺ����������Ϊ5.12 g������ʱ��������ƷӦ���Դ�������������·ת��0.08 mol����
D. ����Ĥ����ⱥ��NaCl��Һԭ��ͼ�У����ӽ���ĤӦΪ�����ӽ���Ĥ
����Ĥ����ⱥ��NaCl��Һԭ��ͼ�У����ӽ���ĤӦΪ�����ӽ���Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ�������ں�pH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p��CP������p��CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K����ʵ�顣ʵ����p��CP��Ũ����ʱ��仯�Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ�������

A.�����ɵã����ⷴӦ��50��150s�ڵķ�Ӧ���ʣ�v��pCP����8.0��10��6molL��1s��1
B.�����¶ȣ������ڼӿ콵�ⷴӦ���ʣ����¶ȹ��߷�Ӧ�����ֻ����
C.��Ŀ��Ϊ̽����Һ��pH�Խ��ⷴӦ���ʵ�Ӱ��
D.298K�£��л���p��CP��������pH��10ʱ��pH��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������¼����ǽ�����ϳɰ���ҵ��������ԭ��������ȥ����COһ���·�������ԭ���ɷ�Ϊ�״�������黯�������֡�
�״�����CO��g��+2H2��g��CH3OH��g������H1����116kJmol��1
���黯��CO��g��+3H2��g��CH4��g��+H2O��g����H2����203kJmol��1
��1�����д�ʩ��������ߴ���������COת���ʵ���_____��
A����ʱ�����CH3OH B���ʵ����߷�Ӧ�¶�
C��ʹ�ø�Ч�Ĵ��� D���ʵ�����ѹǿ
��2���״���ƽ�ⳣ��![]() ��ʾ����Ϊƽ������и����ʵ����ʵ�����������CO��H2���ԭ������CO���������Ϊ1%�����״�����CO��ƽ��ת����Ϊw����K����_____���ú�w�ı���ʽ����ʾ��
��ʾ����Ϊƽ������и����ʵ����ʵ�����������CO��H2���ԭ������CO���������Ϊ1%�����״�����CO��ƽ��ת����Ϊw����K����_____���ú�w�ı���ʽ����ʾ��
��3������a��b���ִ����ڲ�ͬѹǿ���¶������£��״��������д�Ч����ͼ��

����ͼ��֪ѡ�����ִ����Ϻ�_____����a��b����������_____��
��4�����й��ڴ���������˵����ȷ����_____��
A���״�������黯�������κ������¾�Ϊ�Է���Ӧ
B��ѡ��ͬ�Ĵ������Կ��ƴ��������������ɼ״������İٷֺ���
C�����¶��뷴Ӧ�������һ��ʱ����ԭ�����м����������������壬���������ƽ��ת������״��IJ���
D���ʵ�������������H2�İٷֺ�������������ߴ���������COƽ��ת����
����������ˮ���Ρ����㽭��ˮ�ijɹ��䷶�����к�����ˮ��������ˮ������һ����Ҫ���⣬ͼ3�Ǹߺ��裨CN������ˮ����������

��5���ߺ����ˮ����ͨ����ⷨ���д�����������Ӧ�������Σ���һ�ε缫��Ӧʽ��CN��+2OH����2e����CNO��+H2O����д���ڶ��εĵ缫��Ӧʽ_____��
��6������ͺ����ˮͨ����ѧ���������������ڼ��������¼���NaClO����CN������Ϊ̼������Ի����Ѻ����塣��д��������ӷ�Ӧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ���������ڴ����а���ȼ��![]() ijУ��ѧС��ѧ���������װ��
ijУ��ѧС��ѧ���������װ��![]() ͼ�����еȼг�װ������ȥ
ͼ�����еȼг�װ������ȥ![]() ���а����������ڲ�ͬ�����·�Ӧ��ʵ�飻
���а����������ڲ�ͬ�����·�Ӧ��ʵ�飻

(1)������������ˮ����ˮ��Һ������ˮ����______�ԣ���ʹʯ����Һ��______����ԭ��Ϊ____________![]() �û�ѧ����ʽ�͵��뷽��ʽ��ʾ
�û�ѧ����ʽ�͵��뷽��ʽ��ʾ![]()
(2)ͼ����ʵ������ȡ����������İ�����װ��ͼ��д�����Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ![]() ����ʵ���ҳ���ҩƷ�ư���
����ʵ���ҳ���ҩƷ�ư���![]() ��______��A������ҩƷΪ______����������Ϊ______��
��______��A������ҩƷΪ______����������Ϊ______��
(3)�������İ��������������ͨ��װ�����У��þƾ���Ƽ��Ⱥ��Թ�������Ϊ______ɫ�����������Ļ�ѧ����ʽ��______
(4)��������������ײ����İ����ֱ��a��b���ܽ�����ͨ�뵽װ�ñ��У�����b���϶˵�ȼ����������������Ϊ��������Ҫ�ɷ�֮һ��
![]() ������ͨ����Ⱥ�˳����______��
������ͨ����Ⱥ�˳����______��![]() ����ȼ�յĻ�ѧ����ʽ��______��
����ȼ�յĻ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����BaO2�����ܱյ����������,��Ӧ2BaO2(s)![]() 2BaO(s)+O2(g)�ﵽƽ��,�����¶Ȳ���,��Сһ���ݻ�,��ϵ���´ﵽƽ��,����˵������ȷ����
2BaO(s)+O2(g)�ﵽƽ��,�����¶Ȳ���,��Сһ���ݻ�,��ϵ���´ﵽƽ��,����˵������ȷ����
A. �����ƽ��Ħ���������� B. BaO����С
C. BaO2��ת���ʼ�С D. ������ܶȼ�С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com