
【题目】图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A、C、D均为无色气体.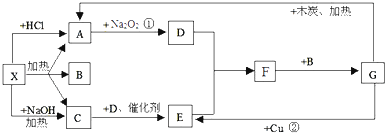
(1)写出有关的物质化学式.X: C: E: F:
(2)写出反应①的化学方程式
(3)写出反应②的离子方程式
【答案】
(1)(NH4)2CO3或NH4HCO3;NH3;NO;NO2
(2)2CO2+2Na2O2=2Na2CO3+O2
(3)8H++2NO3﹣+3Cu═3Cu2++2NO↑+4H2O
【解析】解:X既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,则C为NH3 , 气体A能与过氧化钠反应,故A为CO2 , 则A应为碳酸铵或碳酸氢铵,B为H2O,结合转化关系可知,D为O2 , E为NO,F为NO2 , G为HNO3。
(1)由上述分析可知,X为(NH4)2CO3 或NH4HCO3 , C为NH3 , E为NO,F为NO2 ,
所以答案是:(NH4)2CO3 或NH4HCO3;NH3;NO;NO2;(2)反应①为Na2O2和CO2的反应,反应的化学方程式为:2CO2+2Na2O2═2Na2CO3+O2 ,
所以答案是:2CO2+2Na2O2=2Na2CO3+O2;
(3)反应②是铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式为:3Cu+8H++2N03﹣=3Cu2++2NO↑+4H2O,
所以答案是:3Cu+8H++2N03﹣=3Cu2++2NO↑+4H2O.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】下列各种方法中:①金属表面涂抹油漆 ②改变金属内部结构 ③保持金属表面清洁干燥 ④在金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜,能对金属起到防护或减缓腐蚀作用的是
A.全部 B.①③④⑤ C.①②④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质相互混合后,会发生反应的是
A. CO2和CaCl2溶液 B. Ca(OH)2和硫酸
C. Na2SO4溶液和MgCl2溶液 D. Na2CO3溶液和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( ) 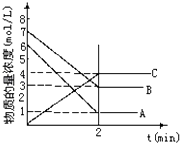
A.该反应的化学方程式为5A+4B4C
B.2min时,该反应达到平衡,此时A,B,C的浓度比为5:4:4
C.用B的浓度变化表示2min内的速率为2mol/(Lmin)
D.2min前,正反应速率逐渐减小,逆反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5 种短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子.试回答下列问题:
(1)用电子式表示离子化合物A2B的形成过程:
(2)写出下列物质的电子式:D元素形成的单质;B与E形成的化合物;A、B、E形成的化合物;D、E形成的化合物 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对无水乙醇与金属钠的反应进行实验探究。请回答:
实验装置 | 操作步骤 | 实验现象 |
| ①用橡胶管将尖嘴管和仪器a连接,向仪器a的球形区域塞入一团脱脂棉,再向脱脂棉中滴入适量的酸性K2Cr2O7溶液 | 棉花呈橙黄色 |
②取黄豆大小的金属钠,用滤纸吸干其表面的煤油,放入小烧杯中,用仪器a的柱体部分扣住金属钠,再向小烧杯中倒入10mL左右无水乙醇,至高度没过金属钠 | ||
③反应开始20s左右,点燃尖嘴管处的气体,并在尖嘴管上方罩上内壁涂有澄清石灰水的小烧杯 | 产生明亮的淡蓝色火焰,仪器a内的脱脂棉逐渐由橙黄色变为绿色(Cr3+颜色),烧杯内壁未变浑浊 | |
④实验结束后测量反应液的温度 | 反应液的温度为52℃ |
(1)仪器a的名称是_____。
(2)请写出无水乙醇与钠反应的化学方程式:_____。
(3)下列有关该实验的说法中,正确的是_____。
A.无水乙醇与钠的反应是吸热反应
B.酸性重铬酸钾溶液的作用是除去乙醇蒸气中混有的氢气
C.仪器a的球形区域对产生的气体起到一定的富集作用,使得气体燃烧的火焰明亮,现象明显
D.操作步骤②中的现象有:加入无水乙醇后,钠表面有气泡,钠开始时沉在液体的底部,然后浮在液面上,直至消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。(Sn: 119)
回答下列问题:
(1) 操作Ⅰ是________、过滤洗涤。
(2)SnCl2粉末需加浓盐酸进行溶解,目的是_______________________________。
(3)加入Sn粉的作用有两个:①调节溶液pH,②____________________________。[
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是___________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl![]() SnCl2+ H2↑;
SnCl2+ H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2+ K2Cr2O7+ 14HCl![]() 6FeCl3+ 2KCl + 2CrCl3+7H2O
6FeCl3+ 2KCl + 2CrCl3+7H2O
现取0.80 g锡粉,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液20.00mL。则锡粉中锡的纯度为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com