
【题目】部分氧化的Fe﹣Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理: 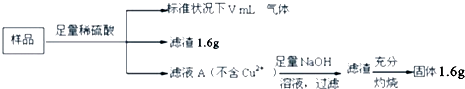
下列说法错误的是( )
A.滤液A中不含Fe3+
B.样品中含氧元素的物质的量为0.01mol
C.上图中V=112
D.溶解样品的过程中消耗的硫酸的总的物质的量为0.02mol
【答案】C
【解析】解:A.与硫酸反应后有滤渣,一定含Cu、则滤液A中一定不含Fe3+ , 故A正确;B.滤渣1.6g为金属铜,物质的量为0.025mol,即合金样品中总共含有铜元素0.025mol,滤液A中加入足量氢氧化钠溶液,所得滤渣灼烧得到的固体1.6g为Fe2O3 , 物质的量为0.01mol,铁元素的物质的量为0.02mol,合金中Fe元素质量=0.02mol×56g/mol=1.12g,Cu元素质量为1.6g,故合金中氧原子的物质的量 ![]() =0.01mol,故B正确;
=0.01mol,故B正确;
C.只有Fe与硫酸反应生成氢气,由Fe+H2SO4=FeSO4+H2↑、Fe+Fe2O3+3H2SO4=3FeSO4+3H2O可知,参加反应硫酸物质的量为0.02mol,硫酸含氢离子0.04mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,它结合氢离子0.02mol,所以硫酸中有0.04mol﹣0.02mol=0.02mol H+生成氢气,即生成0.01mol氢气,标况体积=0.01mol×22.4L/mol=0.224L=224mL,故C错误;
D.滤液A溶质为过量H2SO4和FeSO4 , 而铁元素物质的量为0.02mol,说明参加反应硫酸物质的量为0.02mol,故D正确;
故选C.


 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】PVC是聚氯乙烯的英文缩写,为保证PVC塑料制品的性能,通常需要加入多种有机助剂。下列选项中的事实均能支持“PVC保鲜膜对人体健康带来危害”假设的是( )
①PVC塑料属于高分子材料
②使用的有机助剂有毒
③含氯的化合物不一定有毒
④在高温下会分解出有害物质
A.①②
B.③④
C.②④
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:【实验一】焦亚硫酸钠的制取
采用如图1装置(实验前已除尽装置内的空气)制取Na2S2O5 . 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O5 . 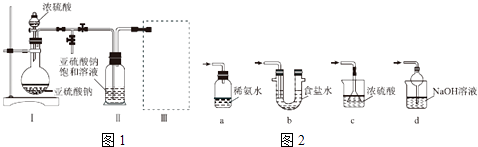
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为(填序号).
(4)【实验二】焦亚硫酸钠的性质:Na2S2O5溶于水即生成NaHSO3 . 证明NaHSO3溶液中HSO ![]() 的电离程度大于水解程度,可采用的实验方法是(填序号).
的电离程度大于水解程度,可采用的实验方法是(填序号).
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
(6)【实验三】葡萄酒中抗氧化剂残留量的测定葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:![]()
(已知:滴定时反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为gL﹣1 .
②在上述实验过程中,若有部分HI被空气氧化,则测定结果(填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为___________________,其原子核外共有_____种运动状态不相同的电子。金属钛晶胞如下图2所示,为________________堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________。
A.180° B.接近120°,但小于120°
C.接近120°,但大于120° D.接近109°28’,但小于109°28’
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为______晶体。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图1。化合物乙的沸点明显高于化合物甲,主要原因是___________________________。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为__________________。

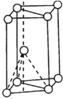
图1 图2
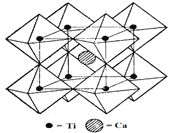
(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被_______个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被__________个氧离子包围。钙钛矿晶体的化学式为_______。若该晶胞的边长为a pm,则钙钛矿晶体的密度为______________g.cm-3(只要求列算式,不必计算出数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N的质量数为14,在粒子NH3T+中,电子数、质子数、中子数之比为
A. 10∶7∶11B. 10∶11∶8C. 10∶11∶9D. 11∶9∶10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_________________________。
(2)烧杯间填满碎纸条的作用是________________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值___________(填“偏大、偏小、无影响”)
(4)如果用50mL0.50mol/L硝酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_________________(填“相等、不相等”),所求中和热__________(填“相等、不相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题.
(1)流程甲加入盐酸后生成Al3+的离子方程式为 .
(2)流程乙加入烧碱后生成SiO ![]() 的离子方程式为 .
的离子方程式为 .
(3)验证滤液B含Fe3+ , 可取少量滤液并加入(填试剂名称)
(4)滤液E、K中溶质的主要成分是(填化学式),写出该溶质的一种用途. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在强碱性溶液中可以大量共存的是( )
A. K+、Na+、HCO3-、Cl-B. Na+、Ba2+、AlO2-、NO3-
C. NH4+、K+、Cl-、NO3-D. K+、Na+、Cu2+、S2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com