
【题目】生态农业涉及农家肥料的综合利用。某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体8.96L(标准状况)。该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO ![]() CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求:
CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求:
(1)原混合气体中甲烷的体积(标准状况)(写出计算过程)
(2)反应后的气体中CO2的物质的量可能为___________
(3)原混合气体中氮气的体积为__________。
【答案】(1)1.68L;(2)0.1mol;0.3mol(3)2.24L或6.72L。
【解析】
试题分析:玻璃管内减少的质量是CuO中氧元素的质量,所以n(CuO) = 4.8g ÷ 16 g/mol = 0.3mol,则根据方程式可知n(CH4) = 1/4n(CuO) = 1/4 × 0.3mol = 0.075mol,其体积是V(CH4)=0.075mol×22.4L/mol=1.68L;发生该反应产生的CO2的物质的量与甲烷的物质的量相等,也是0.075mol,将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。n[Ca(OH)2]= 2L×0.lmol/L=0.2mol,反应产生的CaCO3的物质的量是n(CaCO3)=10g÷100g/mol=0.1mol<0.2mol,可能是石灰水过量,二氧化碳不足量,则n(CO2)= n(CaCO3)=0.1mol;也可能是CO2过量,将Ca(OH)2完全发生反应:Ca(OH)2+ CO2=CaCO3↓+H2O,消耗CO20.2mol,产生CaCO30.2mol,然后又发生反应:CaCO3+ CO2+H2O =Ca(HCO3)2,由于最后CaCO3的物质的量是0.1mol,所以发生上述反应消耗CO2的物质的量是0.1mol,则反应后CO2气体的物质的量也可能是0.2mol+0.1mol=0.3mol;(3)若二氧化碳全部转化为CaCO3,生成10g沉淀是CaCO3,碳酸钙的物质的量为:10g÷100g/mol=0.1mol,故反应后的二氧化碳总的物质的量为0.1mol,甲烷反应生成的二氧化碳的物质的量为0.075mol,故原混合气体中二氧化碳的物质的量为0.1mol-0.075mol = 0.025mol,原混合物中CO2的体积为0.025mol×22.4L/mol=0.56L,故原混合气体中氮气的体积为:8.96L-1.68L-0.56L=6.72L;若二氧化碳部分转化为CaCO3,生成10g沉淀是CaCO3,物质的量为0.1mol,根据钙离子守恒可知转化生成的Ca(HCO3)2的物质的量为:2L×0.1mol/L-0.1mol=0.1mol,故反应后的二氧化碳总的物质的量为0.1mol+0.1mol×2=0.3mol,甲烷反应生成的二氧化碳的物质的量为0.075 mol,故原混合气体中二氧化碳的物质的量0.3mol-0.075mol=0.225mol,原混合物中CO2的体积为0.225mol×22.4L/mol=5.04L,故原混合气体中氮气的体积为:8.96L-1.68L-5.04L=2.24L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系(反应中生成的水已略去)。
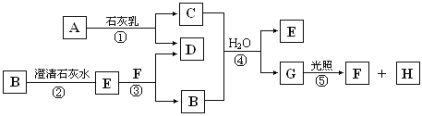
请回答以下问题:
(1)E是 (填化学式),G是 (填名称);
(2)C物质在日常生活中可作 ;
(3)写出反应①的化学方程式 ;
C与浓盐酸反应,可以生成A气体,写出反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________。
(2)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为______________。
(3)联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究.其结构简式如图.下列关于分枝酸的叙述正确的是( )

A.1mol分枝酸最多可与3molNaOH发生中和反应
B.可与乙醇、乙酸反应,且反应类型相同
C.分子中含有2 种官能团
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色.且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(g)N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用止水夹夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示.与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅.下列说法错误的是
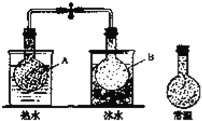
A. 上述过程中,A烧瓶内正、逆反应速率均加快
B. 上述过程中,B烧瓶内c(NO2)减小,c(N2O4)增大
C. 上述过程中,A、B烧瓶内气体密度均保持不变
D. 反应2NO2(g)N2O4(g)的逆反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用纯净的KCl固体,但目前只有含K2SO4、(NH4)2CO3杂质的KCl。某学生设计了如图所示方案进行提纯。
已知:1.(NH4)2CO3![]() 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
2.K2SO4、KCl热稳定性好,KCl溶解度随温度变化不大;
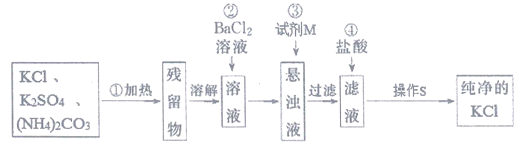
根据以上信息,回答下列问题:
(1)步骤①加热的目的是:______________;此操作可选择在______________(填仪器名称)中进行;
(2)步骤②不用硝酸钡溶液,其理由是_________________;
(3)进行步骤②时,简述判断SO42-是否除尽的实验操作、现象和结论:____________;
(4)步骤③所加试剂M为:_______________,其目的是_________________;
(5)操作S的名称是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类、脂肪和蛋白质的叙述正确的是
A. 蛋白质溶液遇CuSO4后产生的沉淀能重新溶解 B. 淀粉水解的最终产物是葡萄糖
C. 葡萄糖能发生氧化反应和水解反应 D. 植物油不能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是
A. 任何气体单质在标准状况下体积约为22.4L,则一定含有2NA个原子
B. 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA
C. 常温常压下,22.4LH2O中含有的氢原子数为2NA
D. 标准状况下,0.3molCO2中含有氧原子数0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com