
【题目】亚硝酸钠(NaNO2)既可以作氧化剂又可以作还原剂,当它在反应中作氧化剂时,可能生成的产物是( )
A.N2B.N2O3C.HNO3D.NO2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】锰及其化合物在生产、生活中有许多用途。在实验室中模拟工业利用软锰矿(主要成分为MnO2,含少量SiO2、Fe2O3和Al2O3等)制备金属锰等物质,设计流程如下:

己知:Mn2+有较强的还原性,在空气中能被氧气氧化,碳酸锰在空气中高温加热固体产物为Mn2O3;部分氢氧化物的Ksp(近似值)如下表。
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
(1)“酸浸”前需将软锰矿粉碎的目的是_____________;酸浸过程MnO2发生反应的离子方程式为_________________。
(2)向滤液I中需先加A物质,再加B物质,若加入的物质均为非金属化合物的溶液,则A为(填物质的名称)_________,B为(填物质的名称)________。滤渣II的成分是_______(填物质的化学式)。
(3)“酸浸”需适宜的酸浓度、液固比、酸浸温度等,其中浸取率随酸浸时间的变化如图所示:

当浸取时间超过4h时,锰浸取率反而减小,其原因是______________。
(4)测得滤液I中c(Mn2+)=0.1mo/L,则加入B调节溶液pH范围为______。(已知:当某种离子浓度小于1×10-5mo/L时,可认为其沉淀完全。结果保留两位小数)
(5)“沉锰”过程中加入氨水的目的是(从化学平衡移动的角度解释)______________。
(6)写出由MnCO3为原料制备金属锰的过程中所涉及的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作(注意事项)中,是基于实验安全考虑的是( )
①加热盛有液体的烧瓶时,需加碎瓷片或沸石
②酒精灯内的酒精不能小于酒精灯容积的三分之一
③实验前,要对气体实验装置进行气密性检査
④稀释浓硫酸时,将浓硫酸沿烧杯内壁慢慢注入水中
⑤实验结束后,清洗后的洁净试管,要倒放在试管架上
A. ①②③④⑤ B. ①②④ C. ②③④ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作(注意事项)中,是基于实验安全考虑的是( )
①加热盛有液体的烧瓶时,需加碎瓷片或沸石
②酒精灯内的酒精不能小于酒精灯容积的三分之一
③实验前,要对气体实验装置进行气密性检査
④稀释浓硫酸时,将浓硫酸沿烧杯内壁慢慢注入水中
⑤实验结束后,清洗后的洁净试管,要倒放在试管架上
A. ①②③④⑤ B. ①②④ C. ②③④ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

Ⅰ.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙___________;
(2)氯化钠溶液中分离出氯化钠___________;
(3)分离植物油和水___________;
(4)海水淡化___________;
(5)氯化钠溶液中分离出水___________;
(6)除去自来水中的Cl﹣等杂质___________;
(7)从碘水中分离出I2___________。
Ⅱ.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是___________。
A.酒精 B.苯
②分液漏斗在使用前必须先___________。
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的______端口放出,有机层应由分液漏斗的______端口放出(此问填“上”或者“下”)
(2)蒸馏
①装置A中a的名称是_______,冷凝装置中冷凝水应该________口进(填“上”或“下”),这样做的目的是________________________,装置C在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是__________________________。
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是___________。
Ⅲ. 海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题一:粗盐中含Ca2+、Mg2+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发正确的操作顺序是__________(填选项字母).
⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
问题二:由海水到氯化钠晶体的实验过程中要用到的主要装置是_________________(从给定的四种装置中选择,填字母)。
问题三:粗盐中含有少量泥沙、CaCl2、MgCl2及硫酸盐,将粗盐溶解后,先过滤将泥沙除去,再检验滤液中的SO42﹣,检验滤液中的SO42﹣的实验操作和现象是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
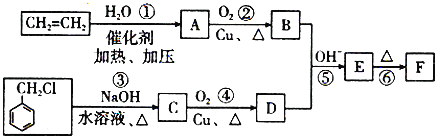
【题目】肉桂醛F(![]() )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
已知两个醛分子在NaOH溶液作用下可以发生反应,生成一种羟基醛:
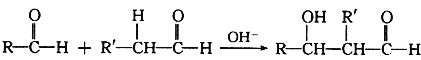
请回答:
(1)D的结构简式为______.
(2)反应①~⑥中属于加成反应的是______(填序号).
(3)写出有关反应③的化学方程式:___________.
(4)在实验室里鉴定![]() 分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是______(请按实验步骤操作的先后次序填写序号).
分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是______(请按实验步骤操作的先后次序填写序号).
A.滴加AgNO3溶液B.加NaOH溶液C.加热D.用稀硝酸酸化
(5)E物质的同分异构体有多种,其中符合条件:苯环上有两个取代基,其中一个是羧基的为:______(写出其中一种同分异构体的结构简式即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
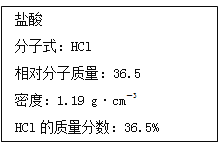
(1)该浓盐酸中HCl的物质的量浓度为______ mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸加蒸馏水稀释至500 mL,得到物质的量浓度为0.400 mol·L-1的稀盐酸。该学生需要量取________ mL上述浓盐酸进行配制。
(4)假设该同学用0.400 mol·L-1的盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com