
【题目】下列关于原子结构、元素性质的说法正确的是
A. 含有金属元素的化合物中一定含离子键
B. VIIA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
C. 同种元素的原子均有相同的质子数和中子数
D. IA族金属元素是同周期中金属性最强的元素
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在强酸性溶液中,下列各组离子一定能大量共存的是
A.Cl-、Cu2+、SO42-、NO3- B.OH-、Na+、SO42-、CH3COO-
C.Cl-、Fe2+、MnO4-、NO3- D.AlO2-、Na+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)某探究小组以硫酸和铜为原料设计如下四种制备硫酸铜晶体的路线:

请回答下列有关问题:
(1)甲方案中第一步发生反应的化学方程式为___________________。
(2)甲、乙、丙方案中,_____方案更合理,原因是________________。
(3)采用乙方案,用废铜、废酸(含HNO3、H2SO4)为主要原料制备硫酸铜晶体,某含有c(HNO3)=2molL-1,c(H2SO4)=4molL-1的废酸混合液100mL(不使用其它酸或氧化剂),最多能制备硫酸铜晶体(CuSO4 5H2O)的质量为___________。
(4)丙方案中灼烧时,应在________中进行(填仪器名称),该实验中的后续操作指的是____________。
(5)丁方案中X可以是试剂,也可以是反应条件:
①若X为试剂,该反应的化学方程式为__________________。
②若X为反应条件,即通电,在虚线框中画出该实验设计图。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据钠与水(滴有酚酞溶液)反应的实验现象,不能得出的结论是 ( )
A. 钠的密度比水小 B. 钠的硬度小
C. 钠很活泼,易与水反应生成碱性物质 D. 钠的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】额度图有机物分子中带“*”碳原子是手性碳原子。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是
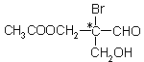
①与甲酸发生酯化反应
②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应
④催化剂作用下与H2反应
A、①②③④ B、①③ C、②④ D、以上反应都不成立
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
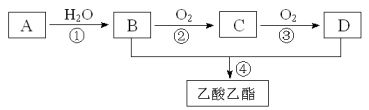
回答下列问题:
(1)写出A的电子式 ,其空间构型 。
(2)B、D分子中的官能团名称分别是 、 ;
(3)写出下列反应的反应类型:② ④ ;
(4)写出A→B反应的化学方程式: ;
(5)写出B与D反应生成乙酸乙酯的化学反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、K+、NH4+、Mg2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,离子浓度都为0.1mol·L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:

则关于原溶液的判断不正确的是
A.若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响
B.无法确定原溶液中是否存在Cl-
C.肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定
D.肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化
物。某化学研究小组利用下列装置加热至高温使FeSO4分解。
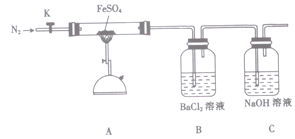
实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通人一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通人氮气至玻璃管冷却。
(2)已知M中铁元素的质量分数为70%,M的化学式为__________。
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置
进行实验。

(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →________ →________。
②能证明生成了非金属氧化物N的现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源危机当前是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法有助于“开源节流”的是________(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
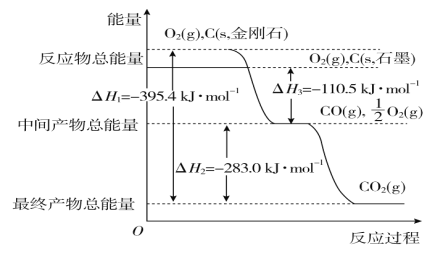
①在通常状况下,金刚石和石墨相比较,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________。
②12 g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为________。
(3)已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
N2(g)+O2(g)===2NO(g) ΔH=+180.0 kJ· mol-1NO分子中化学键的键能为____kJ·mol-1。
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com