
【题目】现有下列十种物质:①Cl2②铝③醋酸(CH3COOH)④CO2⑤H2SO4⑥熔融Ba(OH)2 ⑦氨水⑧稀硝酸⑨Al2(SO4)3固体 ⑩NaHSO4
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是__________;属于弱电解质的是________;属于强电解质的是__________;能导电的是____________。
(2)写出③溶于水时的电离方程式________________________________________。
(3)实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量①。反应方程式为: KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O(未配平)
配平上述反应并用双线桥法标出反应中电子转移的方向和数目:____________________
KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O
【答案】 ④ ③ ⑤⑥⑨⑩ ②⑥⑦⑧ CH3COOH![]() CH3COO-+H+
CH3COO-+H+ 
【解析】(1)溶于水和在熔融状态下均不能导电的化合物是非电解质,因此属于非电解质的是CO2;弱酸、弱碱以及水是弱电解质,则属于弱电解质的是醋酸;强酸、强碱大部分盐是强电解质,属于强电解质的是硫酸、熔融的氢氧化钡、硫酸铝和硫酸氢钠;含有自由移动电子或离子的物质可以导电,则能导电的是铝、熔融的氢氧化钡、氨水、稀硝酸。(2)醋酸是弱酸,部分电离,溶于水时的电离方程式为CH3COOH![]() CH3COO-+H+。(3)根据方程式可知Mn元素化合价从+7价降低到+2价,得到5个电子。Cl元素化合价从-1价升高到0价,失去1个电子,根据电子得失守恒、原子守恒可知反应中电子转移的方向和数目可表示为
CH3COO-+H+。(3)根据方程式可知Mn元素化合价从+7价降低到+2价,得到5个电子。Cl元素化合价从-1价升高到0价,失去1个电子,根据电子得失守恒、原子守恒可知反应中电子转移的方向和数目可表示为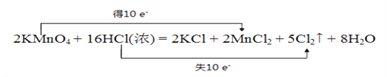 。
。


科目:高中化学 来源: 题型:
【题目】已知元素的原子序数,可以推知原子的①中子数 ②核电荷数 ③核外电子数 ④在周期表中的位置,其中正确的是( )
A. ①③ B. ②③ C. ①②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 金属与非金属元素形成的化合物一定是离子化合物
B. 干冰气化过程中只需克服分子间作用力
C. HF的热稳定性很好,是因为HF分子间存在氢键
D. 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关,下列说法不正确的是
A. 金属钠可以用来冶炼某些金属 B. 镁条着火可以用CO2灭火
C. 石灰石用于工业炼铁和玻璃制造 D. 二氧化硅除可用于制作光学镜片、石英坩埚外,还可用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A. c(NH4+)相等的(NH4)2SO4溶液、NH4HSO4和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2 (SO4)]<c(NH4HSO4)<c(NH4Cl)
B. 欲除去CuCl2溶液中混有少量的FeCl3,可加入CuO
C. 0.2mol/LHCl溶液与等体积0.05 mol/L Ba(OH)2溶液混合后,溶液的pH=1
D. 0.2mol/L的NaHCO3溶液中:c(H+) + c(H2CO3)=c(CO32-) + c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有镁铝合金共3.90克,与500ml 2.00mol/L盐酸(足量)反应,生成的气体在标准状况下体积为4.48L,若反应后所得溶液的体积稀释为1000ml,求:
(1)求镁铝合金中铝的物质的量。
(2)求镁铝合金中镁的质量分数。
(3)求反应后溶液中Cl-的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如下:

请回答下列问题:
(1)已知CeCO3F中C为+4价,Ce元素的化合价为_______。焙烧后Ce元素被________。(填“氧化”或“还原”)
(2)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染。写出稀硫酸、H2O2与CeO2反应的离子方程式:_______________________________。
(3)向Ce(BF4)3中加入KCl溶液的目的是__________________。
(4)CeCl3 .6H2O属于___________物(填“纯净”或“混合物”)
(5)准确称取0.75gCeCl3样品置于锥形瓶中,加入适量过硫酸铵溶液将Ce3+氧化为Ce4+,然后加入25ml 0.10mol/l (NH4)2Fe(SO4)2与之恰好反应完。(已知:Fe2++Ce4+=Ce3++Fe3+)该样品中CeCl3的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所指物质一定属于纯净物的是
A. 常温下的二氧化氮气体
B. 分子式为CH2Cl2的物质
C. 标准状况下,按体积比为1:1混合的NH3和水
D. 只含铁和氧两种元素且Fe的质量分数为72.41%的物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com