
【题目】短周期元素X和Y组成化合物X2Y,那么X和Y所在族的序数不可能分别是
A.ⅠA和ⅦAB.ⅠA和ⅥA
C.ⅦA和ⅥAD.ⅤA和ⅥA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气,下列说法错误的是
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应NH3被还原
D.生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种粒子。其中N2、ClO-的物质的量随时间变化的曲线如图所示。下列判断不正确的是
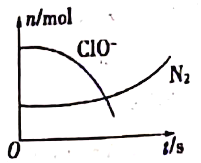
A. 该反应的氧化剂是ClO-
B. 消耗1mol还原剂,转移3mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 该离子方程式为3ClO-+2NH4+=2H++N2↑+3Cl-+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上由ClO2气体制取NaClO2固体的工艺流程如图所示,下列说法错误的是

A. 通入的空气可将发生器中产生的ClO2全部驱赶到吸收器中
B. 吸收器中生成NaClO2的离子方程式为2ClO2+H2O2=2ClO2-+2H++O2↑
C. 步骤a的操作包括过滤、洗涤和干燥
D. 工业上将ClO2气体制成NaClO2固体,其主要目的是便于贮存和运输
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某研究性学习小组设计制取氯气并以氯气为原料进行特定反应的装置。
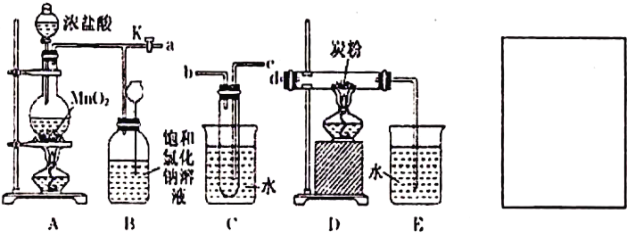
(1)要将C装置接入 B和 D 之间,正确的接法是:a→_________→_________→d;
(2)实验开始先点燃 A处的酒精灯,打开旋塞 K,让 Cl2充满整个装置,再点燃 D处的酒精灯。Cl2通过 C 装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成 CO2和 HCl(g),A 中发生反应的化学方程式为__________________。
(3)D处反应完毕后,关闭旋塞 K,移去两个酒精灯,由于余热的作用,A 处仍有少量 Cl2产生,此时 B 中的现象是___________________________。
(4)用量筒量取 20mLE 中溶液,倒入已检查不漏水的分液漏斗中,然后再注入 10mLCCl4,盖好玻璃塞,振荡,静置于铁架台上(如图),等分层后取上层液和下层液,呈黄绿色的是_________(填“上层液”或“下层液”)。
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列反应方程式:
①CH3-CH2-Br与氢氧化钠溶液在加热条件下的反应方程式 ___________________________________。
②乙醛与银氨溶液水浴加热条件下的反应方程式___________________________________。
③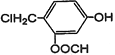 与NaOH溶液在加热条件下的化学反应方程式___________________________________。
与NaOH溶液在加热条件下的化学反应方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废料中含有 Cr(OH)3、Al2O3、CuO、NiO 等物质,工业上通过下列流程回收其中有用的金属和制取 Na2Cr2O7。
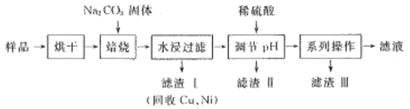
已知:①“水浸过滤”后的溶液中存在 Na2CrO4、NaAlO2 等物质
②除去滤渣 II 后,溶液中存在反应 2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
③Na2Cr2O7、Na2CrO4 在不同温度下的溶解度(g/100 g H2O)如下表:
20℃ | 60℃ | 100℃ | |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
(1)“焙烧”过程中生成 NaAlO2 的化学方程式为_____。
(2)生成滤渣时,需加入适量稀硫酸调节溶液的 pH 除去 AlO2 -,若稀硫酸过量,则因过量引起反应的离子方程式为_______________________。
(3)“系列操作”为:继续加入稀硫酸、_____、冷却结晶、过滤。继续加入稀硫酸的目的是_________;滤渣 III 中除含有少量硫酸钠晶体外,主要成分是 _________________(写化学式)。
(4)工业上还可以在“水浸过滤”后的溶液中加入适量稀硫酸,用石墨作电极电解生产金属铬,阴极的电极反应式为 ____。
(5)流程图最后的“滤液”中仍然有残留的 Na2Cr2O7。Cr 为重金属元素,若含量过高就排入河流中, 会对河水造成重金属污染。为测定“滤液”中的 c(Na2Cr2O7),某实验小组取“滤液”20 mL,加水稀释至 250 mL,再取稀释后的溶液 25 mL 于锥形瓶中,用 c mol/L的 FeSO4 溶液进行氧化还原滴定,到终点 时清耗 FeSO4 溶液体积为 V mL[已知发生的反应为Na2Cr2O7+FeSO4+H2SO4→Na2SO4+Cr2(SO4)3+ Fe2(SO4)3+ H2O(未配平)],则“滤液”中的c(Na2Cr2O7)=_________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物是药物生产的中间体, 其结构简式如下图,下列有关叙述不正确的是
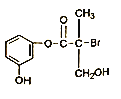
A. 该有机物与浓溴水可发生取代反应
B. 该有机物与浓硫酸混合共热可发生消去反应
C. 1mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH
D. 该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com