
| A�� | ����ˮ�ĵ���̶���С������ˮ�ĵ���̶���� | |
| B�� | ���ڡ��ۻ�ϣ���pH=7����������Һ�������=�� | |
| C�� | ���ķ���Һϡ����ͬ�ı�������Һ��pH���ۣ��ܣ��ڣ��� | |
| D�� | ���١��ܻ�ϣ�����c��CH3COO-����c��H+����������Һһ���ʼ��� |
���� ��ij�¶�ʱ��pH=3��ijˮ��Һ��c��OH-��=10-9 mol/L������¶���ˮ�����ӻ�����K=10-3.10-9=10-12��
��������Һ��pH=6�����¶��£�pH=2�Ĵ�����c��H+��=10-2 mol/L��0.01mol/L������c��H+��=10-2 mol/L��pH=11�İ�ˮ��NaOH��Һ��c��OH-��=0.1mol/L������ˮŨ�ȴ���NaOHŨ�ȣ�
A����������ˮ���룬����������Ũ�Ȼ��������������Ũ��Խ��������ˮ����̶�Խ��
B��������ߵ������ϣ���ˮ��������Һ�ʼ��ԣ���Һ��pH��7��
C��ϡ����ͬ�ı�����pH��6���ڣ��٣��ۣ��ܣ�6��
D�����١��ܻ�ϣ�����c��CH3COO-����c��H+�������ݵ���غ�֪����Һ�д���c��OH-����c��Na+����Ҫ������Һ��c��OH-����c��H+������Դ�С�ж���Һ����ԣ�
��� �⣺��ij�¶�ʱ��pH=3��ijˮ��Һ��c��OH-��=10-9 mol/L������¶���ˮ�����ӻ�����K=10-3.10-9=10-12��
��������Һ��pH=6�����¶��£�pH=2�Ĵ�����c��H+��=10-2 mol/L��0.01mol/L������c��H+��=10-2 mol/L��pH=11�İ�ˮ��NaOH��Һ��c��OH-��=0.1mol/L������ˮŨ�ȴ���NaOHŨ�ȣ�
A����������ˮ���룬����������Ũ�Ȼ��������������Ũ��Խ��������ˮ����̶�Խ�٢���������Ũ����ȡ��ۢ�������������Ũ����ȣ��Ңۡ���������������Ũ�ȴ��ڢ٢���������Ũ�ȣ���������ˮ����̶ȣ��ۢ�С�ڢ٢ڣ���A����
B��������ߵ������ϣ���ˮ���ʵ���ԶԶ�������ᣬ��Һ�ʼ��ԣ���Һ��pH��7����B����
C��ϡ����ͬ�ı�����pH��6���ڣ��٣��ۣ��ܣ�6��������Һ��pH���ۣ��ܣ��ڣ��٣���C��ȷ��
D�����١��ܻ�ϣ�����c��CH3COO-����c��H+�������ݵ���غ�֪����Һ�д���c��OH-����c��Na+���������Һ��c��OH-����c��H+������Һ�ʼ��ԣ������Һ��c��OH-����c��H+��������Һ�����ԣ���D����
��ѡC��
���� ���⿼��������ʵĵ��롢�������Һ�����жϵ�֪ʶ�㣬Ϊ��Ƶ���㣬��ȷ������ʵ����ص��ǽⱾ��ؼ���ע����¶���ˮ�����ӻ���������10-14���״�ѡ����B����������˼ά�����жϼ��ɣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
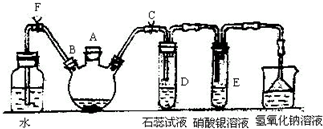 ʵ�����Ʊ��屽������ͼ��ʾ��װ�ã���д���пհף�
ʵ�����Ʊ��屽������ͼ��ʾ��װ�ã���д���пհף� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ������ | Fe��OH��3 | Fe��OH��2 | A1��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 3.4 |
| ��ȫ���� | 3.2 | 9.7 | 4.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| Ũ�ȣ�mol/L�� | a | 0.05 | 0.10 | 0.50 | 0.58 |
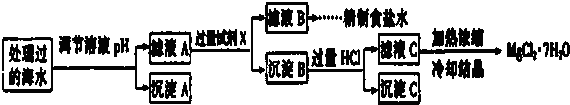
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com