
分析 (1)1-18号元素中金属Na的金属性最强,与氧气反应得到氧化钠、过氧化钠;
(2)金属性最强的元素在周期表的左下角位置,对应的最高价氧化物对应水化物的碱性最强;元素的非金属性越强,对应的最高价氧化物对应的水化物酸性越强;
(3)有机化合物的种类最多,据此判断形成化合物种类最多的元素;
(4)非金属性越强,气态氢化物越稳定.
解答 解:(1)金属性最强的为Na,与氧气反应生成的化合物有:Na2O、Na2O2,
故答案为:Na2O;Na2O2;
(2)金属性最强的元素在周期表的左下角位置,元素周期表1~18号元素中Na的金属性最强,其最高价氧化物对应水化物是NaOH,碱性最强;
Cl的非金属性仅次于O、F,但O、F无正价,最高价氧化物对应的水化物HClO4酸性最强,
故答案为:NaOH;HClO4;
(3)有机化合物的种类最多,主要含C、H元素,
故答案为:C、H;
(4)同周期元素的原子,从左到右得电子能力逐渐增强,氢化物越来越稳定,所以稳定性氨气>甲烷,同主族元素的原子,从上到下得电子能力逐渐减弱,氢化物越来越不稳定,所以稳定性硅烷<甲烷,所以NH3的稳定性强于SiH4,
故答案为:SiH4;NH3.
点评 本题考查元素周期表的结构及应用,题目难度中等,侧重元素在周期表的位置及元素周期律的考查,把握原子半径的比较规律及非金属性的比较方法为解答的关键.


科目:高中化学 来源: 题型:填空题
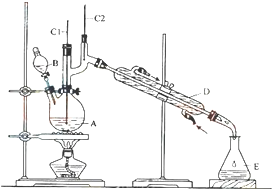 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:| 沸点/0C | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①中水的电离程度最小,③中水的电离程度最大 | |
| B. | 将②、③混合,若pH=7,则消耗溶液的体积②=③ | |
| C. | 将四份溶液稀释相同的倍数后,溶液的pH:③>④>②>① | |
| D. | 将①、④混合,若有c(CH3COO-)>c(H+),则混合溶液一定呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
 ,要想提高苯甲酸的转化率,可以采取的措施是加入过量的甲醇、移去苯甲酸甲酯
,要想提高苯甲酸的转化率,可以采取的措施是加入过量的甲醇、移去苯甲酸甲酯
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol O2和 0.3mol H2O | |
| B. | 0.1mol H2SO4和3.6g H2O | |
| C. | 0.1mol MgSO4•7H2O和0.1mol C12H22O11(蔗糖) | |
| D. | 6.02×1023个CO2与0.1mol KMnO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
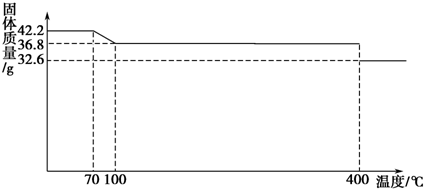
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
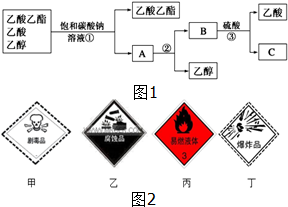 (1)如图1是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,在上述实验过程中,所涉及的三次分离操作的名称分别是①分液②蒸馏③蒸馏.
(1)如图1是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,在上述实验过程中,所涉及的三次分离操作的名称分别是①分液②蒸馏③蒸馏.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂可增大该反应速率 | |
| B. | 增大O2的浓度能加快反应速率 | |
| C. | 该反应达到平衡时,正、逆反应速率相等但不为0 | |
| D. | 一定条件下,2 mol SO2和1 mol O2反应可以得到2 mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.005mol/L的Ba(OH)2溶液,pH=10 | |
| B. | 0.001mol/L的CH3COOH溶液,pH=3 | |
| C. | 0.005mol/L的H2SO4溶液与0.01mol/L的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性 | |
| D. | 完全中和pH=3的H2SO4溶液50ml,需要pH=9的NaOH溶液100ml |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com