
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置 (填代表装置图的字母,下同);除去自来水中的C1等杂质,选择装置 。
(2)从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(3)装置A中①的名称是 ,进水的方向是从 口进水。装置B在分液时为使液体顺利滴下,除打开上口活塞外,还应进行的具体操作是 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
粗盐中含Ca2+、Mg2+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④加入略过量的盐酸 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是 (填写序号)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)用化学方程式回答加入Na2CO3溶液的作用:_____________________。
【答案】(1)D;A(2)B;萃取(分液、蒸馏)
(3)冷凝管;下;将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准漏斗上的小孔
(4)ad(5)CaCl2+Na2CO3=2NaCl+CaCO3↓、BaCl2+Na2CO3=2NaCl+BaCO3↓
【解析】
试题分析:(1)从氯化钾溶液中得到氯化钾固体的方法是蒸发结晶,应选择D装置;除去自来水中的Cl-等杂质的方法是蒸馏,应选择A装置。
(2)从碘水中分离出I2,应该加入苯、四氯化碳等有机溶剂先进行萃取,然后再分液,应选择B装置。
(3)装置A中①的名称是冷凝管,其下口为进水口,上口为出水口;使用分液漏斗分液时,必须先打开分液漏斗上口的玻璃塞或使塞上的凹槽对准漏斗上的小孔,保证内外气压相同,使液体顺利滴下,然后再打开下端的旋塞。
(4)要除去SO42-应选用BaCl2,Ca2+需用Na2CO3除去,NaOH用于除去Mg2+;而过量的BaCl2需用Na2CO3除去;过量的NaOH和Na2CO3需用盐酸除去。所以Na2CO3的作用有两个,既除去Ca2+又除去过量的BaCl2,因此Na2CO3须在BaCl2之后加,而盐酸加在碳酸钠之后,只要满足这两个条件的答案均正确,所以a和d符合。
(5)根据(4)中分析可知碳酸钠的作用是CaCl2+Na2CO3=2NaCl+CaCO3↓、BaCl2+Na2CO3=2NaCl+BaCO3↓。


科目:高中化学 来源: 题型:
【题目】纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域。工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱。其流程如下:

(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉淀,可以向其中加入过量纯碱.此时将混合液中不溶物除去的方法是_______,该操作中所用的仪器有铁架台(带铁圈)、烧杯等,还需要使用的仪器有___________,溶液中多余的纯碱可以加_________试剂来除去。
(2)上述工艺流程中,加压条件下通入二氧化碳进行碳酸化时没有析出碳酸钠晶体,其原因是_________。整个过程中循环利用的物质是________(用化学式表示)。
(3)若采用上述流程生产106吨纯碱,则理论上通入的二氧化碳的体积(标准状况下)不得少于_________L(不考虑二氧化碳的回收利用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3 mol二氧化碳气体中,约含有 个二氧化碳分子;2molNH4+中共有 mol电子,与之电子数相等的H2O的质量是 ,这些水若完全电解,产生的氢气在标准状况下的体积为 L。
(2)相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是 (填化学式,下同),标准状况下体积最大的是 ,原子数最少的是 。
(3)在NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2。如果混合液中共有0.5 mol Cl-,溶液的体积为0.5 L,则混合液中氯化钠的质量为 ;MgCl2的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
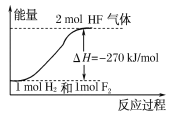
【题目】已知:H2(g)+F2(g)===2HF(g) ΔH=-270 kJ/mol,下列说法正确的是( )
A.氟化氢气体分解生成氢气和氟气的反应是放热反应
B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D.该反应中的能量变化可用如图来表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体体积的叙述中,正确的是( )
A.一定温度和压强下,各种气体物质体积的大小由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的原子数决定
C.无论外界条件是否相同,不同的气体,若物质的量不同,则它们所含的分子数也不同
D.相同状况下,相同微粒数的Fe、H2O、H2的体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与生活相关的叙述错误的是( )
A.酸性臭氧水(AOW)可用于消灭H1N1病毒,因为臭氧具有强氧化性
B.水处理常用到漂白粉和明矾,二者的作用原理相同
C.“地沟油”禁止食用,但可用来制肥皂
D.三聚氰胺添入牛奶中能增加含氮量,但有害健康
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com