
【题目】(1)3 mol二氧化碳气体中,约含有 个二氧化碳分子;2molNH4+中共有 mol电子,与之电子数相等的H2O的质量是 ,这些水若完全电解,产生的氢气在标准状况下的体积为 L。
(2)相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是 (填化学式,下同),标准状况下体积最大的是 ,原子数最少的是 。
(3)在NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2。如果混合液中共有0.5 mol Cl-,溶液的体积为0.5 L,则混合液中氯化钠的质量为 ;MgCl2的物质的量浓度为 。
【答案】(1)1.806×1024;20;36g;44.8
(2)CO2;H2、O2(3)5.85g;0.4mol/L
【解析】
试题分析:(1)3 mol二氧化碳气体中,约含有3mol×6.02×1023/mol=1.806×1024个二氧化碳分子;2molNH4+中共有2mol×10=20mol电子,与之电子数相等的H2O的物质的量是2mol,其质量=2mol×18g/mol=36g,这些水若完全电解,产生的氢气为2mol,在标准状况下的体积为2mol×22.4L/mol=44.8L。
(2)根据![]() 可知在质量相等时气体相对分子质量越大,所含分子数越少,相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是相对分子质量最大的CO2;标准状况下体积最大的是相对分子质量最小的氢气;所含原子的物质的量分别是
可知在质量相等时气体相对分子质量越大,所含分子数越少,相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是相对分子质量最大的CO2;标准状况下体积最大的是相对分子质量最小的氢气;所含原子的物质的量分别是![]() 、
、![]() 、
、![]() ,因此原子数分别是最少的是氧气。
,因此原子数分别是最少的是氧气。
(3)在NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2,设混合液中氯化钠和氯化镁的物质的量分别是xmol、2xmol,则xmol+2xmol×2=0.5mol,解得x=0.1,所以混合液中氯化钠的质量为0.1mol×58.5g/mol=5.85g;MgCl2的物质的量浓度为0.2mol÷0.5L=0.4mol/L。


科目:高中化学 来源: 题型:
【题目】下列各项中物质的类别不正确的是( )
A | B | C | D |
Al2O3 | Si | Na2O2 | Na2SiO3 |
两性氧化物 | 单质 | 碱性氧化物 | 硅酸盐 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A ( C8H8O3)是由冬青树的叶经蒸汽蒸馈而得,因此又名冬青油。它常用作饮 料、牙裔、化妆品的香料,也用作制取止痛药、杀虫剂等。从A出发有如下图所示转化关系 (部分反应产物已略去):
已知以下信息:

已知以下信息:
①A的核磁共振氢谱表明其有六种不同化学环境的氢:且1molA与溴水反应最多消耗 2 mol Br2
② 羧酸盐与碱共热可发生反应,如实验室制甲烷: ![]()
回答下列问题:
(1) K的结构简式为____________________
(2) B→D的反应方程式为_______________________
(3)F→H的反应类型为__________________
按系统命名法H的名称为___________________
(4) A的结构简式为_____________
(5)A的同分异构体中苯环上只有两个取代基且能发生银镜反应和显色反应的共有________种,其中核磁共振氢谱有八种不同化学环境的氢原子的是________ 和_______________ (写结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物![]() 的名称是2,3,5,5-四甲基-4,4-二乙基己烷
的名称是2,3,5,5-四甲基-4,4-二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.甲醛、氯乙烯和乙二醇均可作为合成聚合物的单体
D.乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置 (填代表装置图的字母,下同);除去自来水中的C1等杂质,选择装置 。
(2)从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(3)装置A中①的名称是 ,进水的方向是从 口进水。装置B在分液时为使液体顺利滴下,除打开上口活塞外,还应进行的具体操作是 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
粗盐中含Ca2+、Mg2+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④加入略过量的盐酸 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是 (填写序号)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)用化学方程式回答加入Na2CO3溶液的作用:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟用下图装置测定某粗锌样品中锌的质量分数。他们查阅资料后获知该粗锌样品中的其他成分不能与稀盐酸反应。请填写以下实验报告。
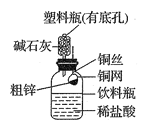
(1)实验目的: 。
(2)实验步骤:
①称取10.0g粗锌置于铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g。
②将铜网插入足量的稀盐酸中,有关反应的化学方程式为 。
③反应完全后,称得装置总质量为119.8g,则粗锌中锌的质量分数为 。
(3)问题探究:(已知碱石灰是NaOH和CaO的混合物,常用于干燥、吸收气体)
①该实验若不用碱石灰,则所测得的粗锌中锌的质量分数将 (填“偏大”、“偏小”或“无影响”);
②若将粗锌换成某含有杂质的石灰石样品(杂质也不与稀盐酸反应),判断该实验方案能不能用于石灰石样品中CaCO3质量分数的测定,并说明理由____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
(1)NO的危害在于 。
a.破坏臭氧层 b.参与酸雨和光化学烟雾的形成
c.与人体内血红蛋白结合 d.当它转化为N2后使空气中O2含量降低
(2)在含有Cu+的酶的活化中心,亚硝酸根离子(NO2-)可转化为NO,写出Cu+和NO2-在酸性溶液中转化为NO的离子方程式 。
(3)一定条件下NO可转化为N2O和另一种红棕色气体,方程式为_____ 。
(4)将0.05molNO、0.03molO2的混合气体以适当的速率缓慢通入盛有100mL水的集气瓶中,最终所得溶液中溶质的物质的量浓度为 (设溶液体积变化忽视不计)。
(5)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2.24L NO 气体.若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com