
| 1000 |
| 25 |
| 1000 |
| 10 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����t1=15s��������C�� t0��t1ʱ��ε�ƽ����Ӧ����Ϊ0.004 mol?L-1?s-1 |
| B��t4��t5�θı������Ϊ��Сѹǿ��t5��t6�θı������������ѧ��Ӧ���¶� |
| C��B����ʼ���ʵ���Ϊ0.02 mol |
| D���û�ѧ��Ӧ�ı���ʽΪ��3A��g��?B��g��+2C��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | �� | �� | �� | �� |
| ϡ�������/mL | 100 | 200 | 300 | 400 |
| ʣ�����/g | 18.0 | 9.6 | 0 | 0 |
| NO���/mL | 2240 | 4480 | 6720 | V |
| A�������ܽ���5.6gFe |
| B������V=6720 |
| C���ٵ��ϲ���Һ�к���Fe2+��Fe3+��Cu2+ |
| D�������Ũ��Ϊ4mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ú��������Һ�����������仯���̣��ɱ�Ϊ�����Դ |
| B���ޡ��顢˿��ë��Ƥ�Լ��ϳ���ά��ȫȼ��ֻ����H2O�� CO2 |
| C�����ع��͡��������Ʊ�������� |
| D��ʯӢ�������ֻ������������֡������������ǹ�������Ʒ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
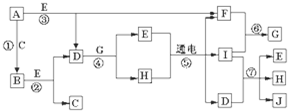
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
C��
| ||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaHCO3��Һ�У�c��H+��+c��H2CO3��=c��OH-�� |
| B��25��ʱ��pH=5.6��CH3COOH��CH3COONa�����Һ�У�c��CH3COO-����c��Na+�� |
| C���ö��Ե缫���NaOH��H2SO4��Ba��OH��2������һ�ֵ���Һʱֻ�������������� |
| D����ˮ�������H+Ũ��Ϊ1��10-12 mol/L����Һ�У�K+��NO3-��I-һ���ܴ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ŵ� |
| ��� |
| A���ŵ�ʱ������ӦΪ��3Zn-6e-+6OH-�T3Zn��OH��2 |
| B���ŵ�ʱOH-�������ƶ� |
| C�����ʱÿת��3 mol���ӣ�������1 mol Fe��OH��3����ԭ |
| D����س������У�KOH�����ʵ���Ũ�Ƚ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com