
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_____________, K值大小与温度的关系是:温度升高,K值______________。(填一定增大、一定减小、或可能增大也可能减小);
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。
CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=_________mol·L-1·min-1。
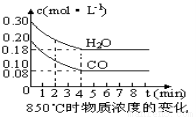
(3)该反应的化学平衡常数表达式为K= _,850℃时当反应进行到4min时即达到平衡状态,这时化学平衡常数的数值为 。
科目:高中化学 来源:2015-2016学年贵州省乌当区新天学校高二上学期期中测试化学试卷(解析版) 题型:?????
当光束通过下列分散系时,能观察到丁达尔效应的是
A.蔗糖溶液
B.Fe(OH)3胶体
C.氯化钠溶液
D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
在同一容器内有X、Y、Z、Q四种物质,在合适的条件下反应,反应前后各物质的质量如表,该反应属
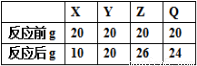
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:填空题
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,丙池是电解精炼铜。
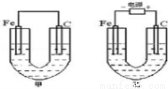
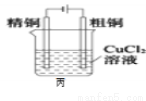
(1)甲池中盛有CuSO4溶液,反应一段时间后,有红色物质析出的是 棒,甲池中铁电极上电极反应式是 。
(2)乙池中盛有饱和NaCl溶液,总反应的化学方程式为 。若往乙池中滴入酚酞试液, 电极(填“Fe”或“C”)附近呈现红色。反应一段时间后,若要使溶液恢复到电解前的状态,可以向溶液中通入一定量的 。
(3)丙池中粗铜电极发生 (填“氧化”或“还原”)反应,反应过程中,Cu2+的浓度 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高一上学期期中测试化学试卷(解析版) 题型:选择题
在Al2(SO4)3、MgSO4、K2SO4的混合溶液中,含有的Al3+ 、Mg2+ 、SO42?的个数比是2∶3∶8,则溶液中Al2(SO4)3、MgSO4、K2SO4的物质的量之比是
A.1∶2∶4 B.2∶3∶2 C. 1∶2∶3 D. 1∶3∶2
查看答案和解析>>
科目:高中化学 来源:2016届山东省潍坊市高三上学期期中测试化学试卷(解析版) 题型:填空题
许多含氯物质与生活密切相关,如HClO、ClO2、NaClO2等都是重要的杀菌消毒剂和漂白剂。其中制备NaClO2的工业流程下图所示:

请回答下列问题:
(1)反应器I中反应的氧化剂是___________________。
(2)反应器Ⅱ中发生反应的离子方程式为_________________________________。
(3)通入反应器Ⅱ中的SO2能用H2O2代替,请简要说明理由____________________。
(4)为了测定NaClO2粗品的纯度,取上述粗产品10.0 g溶于水配成1 L溶液,取出10 mL,溶液于锥形瓶中,再加入足量酸化的KI溶液。充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1Na2S2O3标准液漓定,达到滴定达终点时用去标准液20.00 mL,试计算NaClO2粗品的纯度___________。(提示:2Na2S2O3+I2====Na2S4O6+2NaI)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一上学期期中测试化学试卷(解析版) 题型:填空题
选择下列实验方法分离物质,将正确分离方法的序号填在横线上。
A 萃取 B 升华 C 结晶 D 分液 E 蒸馏 F 过滤
(1)分离饱和食盐水与沙子的混合物__________
(2)提取碘水中的碘单质________
(3)分离水和汽油的混合物________
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
在相同容积的4个密闭容器中进行同一种可逆反应,2A(g)+B(g)  3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示: 各容器所盛物质的量
3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示: 各容器所盛物质的量
容器 | 甲 | 乙 | 丙 | 丁 |
A | 2mol | 1mol | 2mol | 1mol |
B | 1mol | 1mol | 2mol | 2mol |
在相同温度下,建立平衡时,4个容器中A或B的转化率的大小关系是
A.A的转化率为:甲<丙<乙<丁
B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁
D.B的转化率为:丁>丙>乙>甲
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期第二次月考化学试卷(解析版) 题型:填空题
A、B、C、D四种短周期元素,A元素的一种同素异形体是自然界硬度最大的单质,C与A同主族,C元素的原子序数是B的2倍,工业上以D元素的单质与石灰乳为原料制造漂白粉。按要求回答下列问题:
(1)B的原子结构示意图为 ;镁条在气体B中燃烧生成的物质是 (填化学式);
(2)A的非金属性强于C,请用一个化学反应方程式表示_______________;
(3)写出元素D的单质与石灰乳制漂白粉的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com