
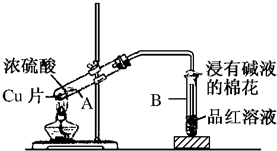
分析 (1)实验室制备气体连接装置后,开始气体制备实验前应先检验装置的气密性;
(2)铜与浓硫酸在加热条件下反应生成二氧化硫,二氧化硫有毒,能引起空气污染,依据二氧化硫为酸性氧化物的性质选择氢氧化钠溶液吸收过量的二氧化硫;
(3)依据二氧化硫的漂白性解答;
(4)铜与浓硫酸在加热条件下反应生成二氧化硫、硫酸铜和水;
(5)依据二氧化硫与碘水反应中硫元素化合价变化判断;
(6)硝酸根离子在酸性环境下具有强的氧化性,能够氧化铜生成硝酸铜,本身被还原为一氧化氮.
解答 解:(1)实验室制备气体连接装置后,开始气体制备实验前应先检验装置的气密性,
故答案为:检查装置的气密性;
(2)铜与浓硫酸在加热条件下反应生成二氧化硫,二氧化硫有毒,能引起空气污染,二氧化硫能够与氢氧化钠溶液反应,被氢氧化钠溶液吸收,防止造成空气污染;
故答案为:吸收SO2,防止污染环境;
(3)二氧化硫具有漂白性,若生成二氧化硫则B中品红溶液褪色;
故答案为:B中品红溶液褪色;
(4)铜与浓硫酸在加热条件下反应生成二氧化硫、硫酸铜和水,方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(5)二氧化硫与碘水反应生成硫酸和氢碘酸,硫元素化合价升高,所以二氧化硫为还原剂,表现还原性,方程式:I2+SO2+2H2O═H2SO4+2HI;
故答案为:还原性,I2+SO2+2H2O═H2SO4+2HI;
(6)硝酸根离子在酸性环境下具有强的氧化性,能够氧化铜生成硝酸铜,本身被还原为一氧化氮,离子方程式:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O.
点评 本题考查了实验室制备二氧化硫及性质检验,明确浓硫酸、二氧化硫的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
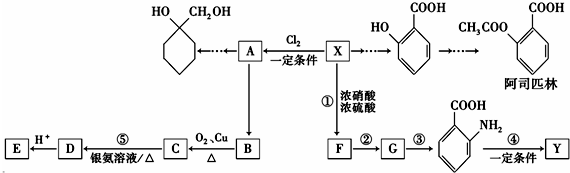

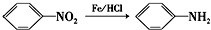 (苯胺,易被氧化)
(苯胺,易被氧化)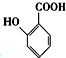 中官能团名称为酚羟基、羧基;
中官能团名称为酚羟基、羧基; ;
; $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$  +(n-1)H2O;
+(n-1)H2O; 的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2
的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2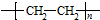
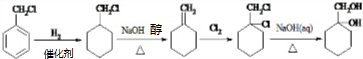 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
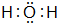 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体中一定存在化学键 | |
| B. | 已知晶胞的组成就可推知晶体的组成 | |
| C. | 分子晶体在晶体态或熔融态下均不导电 | |
| D. | 原子晶体中只存在共价键,不可能存在其他类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有一句正确 | B. | 有两句正确 | C. | 有三句正确 | D. | 四句均正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com