
下列说法正确的是
A.将盐酸和醋酸钠溶液混合后溶液呈中性,溶液中c(Na+)=c(Cl-)
B.1 mol CH4分子中含有的共价键数目等于1 mol Na2O2固体中含有的离子总数
C.80℃的纯水的pH大于25℃的纯水的pH
D.等体积、等物质的量浓度的NaCl溶液中离子总数大于NaClO溶液中离子总数
D
【解析】
试题分析:A.根据电荷守恒可得c(Na+)+C(H+)=c(Cl-)+C(CH3COO-)+C(OH-),若混合溶液显中性,C(H+)=+C(OH-)。两式相减可得c(Na+=c(Cl-)+C(CH3COO-)。错误。B. 1 mol CH4分子中含有的共价键数目为4NA, 1 mol Na2O2固体中含有的离子总数2 NA,二者不等。错误。C.升高温度促进水的电离,是水的离子积常数变大。所以80℃的纯水的pH小于25℃的纯水的pH。错误。D. 在 NaCl的溶液中 [Na+]+[H+]=[Cl-]+[OH-] 离子总数是阳离子的两倍;在NaClO溶液中 [Na+]+[H+]=[ClO-]+[OH-] 离子总数是阳离子两倍与此同时 HClO是弱酸 其酸根离子在水中水解 所以 NaClO溶液呈现微弱的碱性 所以 NaClO中的 [H+]比NaCl的小 所以 其水溶液中的离子总数小综上所述 等物质量浓度,等体积的两种溶液中 NaCl的离子总数更多。正确。
考点:考查溶液中离子浓度的比较及溶液的酸碱性的知识。


科目:高中化学 来源: 题型:阅读理解

| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
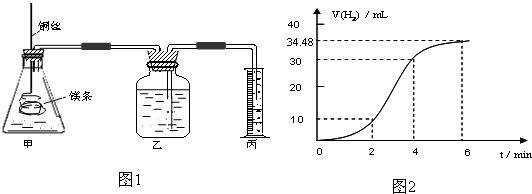
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com