
固体NH4I放入一个体积为VL的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s) NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) H2(g)+I2(g)。平衡时,测得容器中气体共为5mol,其中HI为1.5mol,则下列说法正确的是(
)
H2(g)+I2(g)。平衡时,测得容器中气体共为5mol,其中HI为1.5mol,则下列说法正确的是(
)
A.平衡时氨气为2.5mol
B.平衡时HI的分解率为20%
C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol
D.其他条件不变把容器的体积缩小到V/2 L,重新达到平衡时H2的浓度是原平衡的2倍
科目:高中化学 来源:2010-2011学年河北省高三上学期第四次月考化学试卷 题型:选择题
固体NH4I放入一个体积为V L的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s)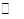 NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) 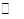 H2(g)+I2(g)。平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是 ( )
H2(g)+I2(g)。平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是 ( )
A.平衡时氨气为2.5 mol
B.平衡时HI的分解率为20%
C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol
D.其他条件不变,把容器的体积缩小到L,重新达平衡时H2的浓度是原平衡的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
固体NH4I放入一个体积为V L的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s)![]() NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) ![]() H2(g)+I2(g)。平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是 ( )
H2(g)+I2(g)。平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是 ( )
A.平衡时氨气为2.5 mol
B.平衡时HI的分解率为20%
C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol
D.其他条件不变,把容器的体积缩小到L,重新达平衡时H2的浓度是原平衡的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
固体NH4I放入一个体积为V L的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s)NH3(g)+HI(g);2HI(g)
H2(g)+I2(g)。平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是 ( )
A.平衡时氨气为2.5 mol
B.平衡时HI的分解率为20%
C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol
D.其他条件不变,把容器的体积缩小到L,重新达平衡时H2的浓度是原平衡的2倍
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省高安中学高二下学期期中考试化学试卷(带解析) 题型:单选题
固体NH4I放入一个体积为VL的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s) NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) H2(g)+I2(g)。平衡时,测得容器中气体共为5mol,其中HI为1.5mol,则下列说法正确的是( )
H2(g)+I2(g)。平衡时,测得容器中气体共为5mol,其中HI为1.5mol,则下列说法正确的是( )
| A.平衡时氨气为2.5mol |
| B.平衡时HI的分解率为20% |
| C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol |
| D.其他条件不变把容器的体积缩小到V/2 L,重新达到平衡时H2的浓度是原平衡的2倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com