
【题目】向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。___
(2)若通入CO2气体为2.24L(标准状况下),得到9.5g的白色固体。
①请通过计算确定此白色固体组成为___。
②所用的NaOH溶液的物质的量浓度为___mol·L-1。
【答案】①NaOH和Na2CO3;②Na2CO3;③NaHCO3;④Na2CO3和NaHCO3 Na2CO3和NaHCO3 1.5
【解析】
向100mLNaOH溶液中缓慢通入一定量的CO2气体,可能发生以下两个反应:
2NaOH+CO2(少量)=Na2CO3+H2O NaOH+CO2(过量)=NaHCO3
(1)NaOH溶液中通CO2,可能发生以下两个反应,若刚好发生前面的一个反应,则反应产物为Na2CO3;若刚好发生后面一个反应,则反应产物为NaHCO3;若NaOH过量,则产物为NaOH与Na2CO3的混合物;若对前一反应来说,CO2过量,而对后一反应来说,CO2不足量,则反应产物为Na2CO3和NaHCO3。
(2)若产物为NaOH和Na2CO3或Na2CO3,则m(Na2CO3)=0.1mol×106g/mol=10.6g>9.5g,不合题意;若产物为Na2CO3和NaHCO3或NaHCO3,则平均相对分子质量M=![]() ,则产物为Na2CO3和NaHCO3的混合物。
,则产物为Na2CO3和NaHCO3的混合物。
设Na2CO3的物质的量为x,则NaHCO3的物质的量为0.1-x
则106x+84(0.1-x)=9.5,求得x=0.05mol,再利用Na+守恒,可求出n(Na+),即n(NaOH),从而求出c(NaOH)。
向100mLNaOH溶液中缓慢通入一定量的CO2气体,可能发生以下两个反应:
2NaOH+CO2(少量)=Na2CO3+H2O NaOH+CO2(过量)=NaHCO3
(1)NaOH溶液中通CO2,可能发生以下两个反应,若刚好发生前面的一个反应,则反应产物为Na2CO3;若刚好发生后面一个反应,则反应产物为NaHCO3;若NaOH过量,则产物为NaOH与Na2CO3的混合物;若对前一反应来说,CO2过量,而对后一反应来说,CO2不足量,则反应产物为Na2CO3和NaHCO3。
(2)若产物为NaOH和Na2CO3或Na2CO3,则m(Na2CO3)=0.1mol×106g/mol=10.6g>9.5g,不合题意;若产物为Na2CO3和NaHCO3或NaHCO3,则平均相对分子质量M=![]() ,则产物为Na2CO3和NaHCO3的混合物。
,则产物为Na2CO3和NaHCO3的混合物。
设Na2CO3的物质的量为x,则NaHCO3的物质的量为0.1-x
则106x+84(0.1-x)=9.5,求得x=0.05mol,再利用Na+守恒,可求出n(Na+)=0.05mol×2+0.05mol×1=0.15mol,即n(NaOH)=0.15mol,从而求出c(NaOH)=![]() 。答案为1.5。
。答案为1.5。


科目:高中化学 来源: 题型:
【题目】氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),已知其中一种化合物的化学式为KCuCl3,下列有关说法中错误的是( )
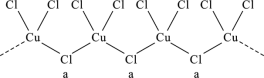
A. a位置上Cl原子的杂化轨道类型为sp3
B. 另一种的化学式为K2CuCl3
C. 铜元素在周期表中位于d区
D. 该物质中存在配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为__________。
(2)下图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为_____。
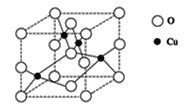
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______________。
(4)Cu2O的熔点比Cu2S的_________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含0.2 molNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含0.5molBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A.0.3mol·L-1B.1.6mol·L-1
C.0.6mol·L-1D.0.8mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A、B是金属单质,E、K是非金属单质,其它为化合物,F、G、H、I、J 焰色反应均为黄色,在这些物质中只有C、K是气体,其中K是黄绿色气体,反应⑧⑨是工业由H制I的重要反应。
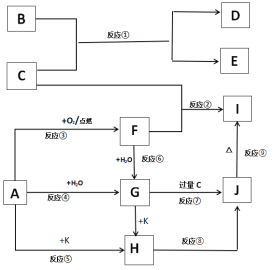
填写下列空白:
(1)写出化学式:B___,F___。
(2)写出反应①的化学反应方程式:____。
(3)写出反应⑦离子反应方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国康乃尔大学的威考克斯(C·Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛像,因而称为释迦牟尼分子(分子中所有原子均在同一平面)如图。对于该有机物的叙述正确的是
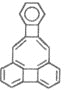
①该有机物属于芳香烃;②该有机物的分子式为C22H12; ③该有机物能发生加成反应;④该有机物的一氯代物的同分异构体有6种
A. ①③④B. ①②C. ②③D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下四种物质:①22g二氧化碳②8g氢气③1.204×1024个氮气分子④4℃时18mL水它们所含分子数最多的是_______,所含原子数最多的______,质量最大的是_____所含电子数最多的是__________(填序号)
(2)12.4 gNa2R含Na+0.4mol,则Na2R的摩尔质量为__________,R的相对原子质量为__________,含R的质量为1.6g的Na2R,其物质的量为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,则下列结论中正确的是

①铜为负极,锌为正极;②铜极上有气泡;③SO42-向铜极移动;④锌发生还原反应;⑤电子的流向是铜到锌;⑥负极反应式:Zn-2e-=Zn2+
A. ①②B. ①④⑥
C. ②④⑥D. ②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知32gA与40gB恰好完全反应,生成mgC和9gD。在相同条件下,16gA和30gB混合反应生成0.25molC及若干摩尔D,则物质C的摩尔质量应是( )
A.63g/molB.122g/molC.126g/molD.163g/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com